血栓预防(专业版)
血栓病是血管内形成异常的血凝块而造成的疾病。血栓形成与血管受损、血液改变和血流淤滞有关。
其他名称:血栓形成;血栓病
英文名称:Blood Clots Prevention,Thrombosis,Thrombotic Disease
根据来源,血栓可分为:
根据血栓形成的部位,血栓又可分为动脉血栓、静脉血栓:
血栓形成及影响因素主要通过如下三种机制中的一种或多种产生:
正常的凝血过程是一系列化学相互作用结果,主要包括血管收缩、血小板栓塞形成阻塞、凝血反应,形成凝块密封孔直到组织修复发生。当受损组织愈合时,不需要的血凝块—坚韧的纤维蛋白链溶解,血液回收凝块的血小板和血细胞。
凝血机制和可干预措施包括如下:
1.血管损伤与收缩:
当血管内皮发生损伤,血管收缩及其附近部位血流减少以利于凝血反应。例如动脉粥样硬化斑块破裂或高同型半胱氨酸所致的内皮损伤。
2.血小板粘附和活化:血小板活化后在血小板之间自我传播、粘附,并靠近在血管壁损伤部位附近。
当循环血小板经过血管壁损伤部位时,则在其周围粘附和结合,这种结合导致血小板活化并可募集更多的血小板。
血小板聚集与可干预路径:血小板激活或活化后,其表面受体可绑定纤维蛋白原形成凝块(约占总血液蛋白4%)。
自然物质干预路径如:
4.凝血反应:纤维蛋白凝胶和血细胞和血小板随后与血小板栓塞融合以加强损伤并完全密封它直到组织修复开始。
4.1.凝血反应过程与可干预路径:在血小板栓塞形成同时,在血管壁损伤时释放的组织因子和胶原蛋白引发两个(内源和外源)的独立但相关的凝血途径,产生更多的凝血酶以转化纤维蛋白:
4.2.纤维蛋白溶解(纤溶):
在血凝完成后(通常在损伤后3-6分钟),凝块内被捕获的血小板开始缩回,凝块收缩更靠近伤口边缘,挤出任何多余的凝血因子。然后,开始修理损伤。一旦愈合,通过纤维蛋白溶解(纤溶)过程溶解并除去不需要的凝块。
深静脉血栓(DVT)症状包括:
调整饮食与生活方式
导致血栓病的原因和风险因素,主要包括高胆固醇、高血压、糖尿病和动脉粥样硬化,以及高同型半胱氨酸血症等,了解更多可点击本网的相关专文内容。
营养与草本综合干预
以下是基于循证医学和循证营养学有关文献综合的结果。
有助于防控血栓病的营养和草本补充剂,主要包括如下:
1.鱼油:
EPA和DHA通过调节血小板和内皮功能来影响止血和血栓形成。EPA和DHA已被证明可降低血小板反应性和聚集性,增加一氧化氮的产生,抑制氧化LDL的产生,并降低内皮细胞表面粘附分子的表达。它们还可以通过减少组织因子的表达来促进纤维蛋白溶解并抑制凝血级联反应1。
一项对八项随机对照试验数据的荟萃分析发现,在稳定和促进冠状动脉动脉粥样硬化斑块消退方面,ω-3脂肪酸联合他汀类药物治疗比单独他汀类药物更有效,可能降低动脉血栓栓塞的风险2。另一项对40项随机对照试验的荟萃分析发现,补充EPA和DHA可降低心脏病发作和心血管死亡的风险,共有135,267名参与者。分析进一步计算出,每天每多摄入1g 的EPA和DHA,心血管事件的风险就会降低5.8%3。
一项利用三项大型队列研究的观察性证据进行的研究表明,血液中DHA水平越高,患动脉粥样硬化性血栓性中风的风险越低,而血液中二十二碳五烯酸(DPA)水平越高则患心脏栓塞性中风(因冠状动脉栓塞引起)的危险越低4。DPA是鱼类中发现的另一种ω-3脂肪酸;它可以在体内由EPA制成,并进一步转化为DHA。
然而,一项对125,763名受试者进行的14项试验的荟萃分析发现,尽管这些试验与心脏病发作和其他主要心血管事件的风险较低有关,但摄入1g或更多的ω-3脂肪酸与出血和发生心房颤动的风险增加有关5。对于有心房颤动病史或有高风险的人,建议谨慎使用鱼油,或遵循医生指导。
一项随机、对照试验对452名因骨折需要腿部手术的老年人进行了研究,发现术后30天服用1g 欧米伽-3脂肪酸可降低深静脉血栓和肺栓塞的风险,且不会增加出血事件或其他并发症6。在567例慢性肾病患者中,连续3个月每天服用4g omega-3脂肪酸可降低用于透析的动静脉瘘急性血栓形成的风险7。一项针对21,970名参与者的观察性研究发现,在中位随访11.6年后,每周从饮食和补充剂中摄入超过4.7g的鱼类omega-3脂肪酸与静脉血栓栓塞风险降低22-26%和肺栓塞风险降低39-60%相关8。较高的omega-3脂肪酸摄入量也与较低的DVT复发率或其他静脉血栓栓塞事件相关,特别是对于那些首次事件没有已知诱因的患者(如手术、住院、癌症或急性疾病)9,10。
2. 辅酶Q10:
辅酶Q10(CoQ10)是一种参与线粒体中还原-氧化平衡和能量产生的营养物质。低CoQ10水平可增加炎症信号传导,并与不良的心血管健康和结果有关,CoQ10补充剂在预防和辅助治疗心血管疾病和相关代谢状况方面具有潜在作用11-14。CoQ10已被发现通过减少动脉壁中氧化的LDL积累来改善血管功能,减少血管损伤和僵硬,增加一氧化氮的可用性13。实验室研究进一步表明,辅酶Q10可以抑制血小板聚集和信号传导,减少血栓生长15。因为使用他汀类药物可降低辅酶Q10的产生,服用他汀类药物的患者尤其可以从补充辅酶Q10中受益14,16。
在一项随机对照试验中,213名低硒老年人连续四年服用200mg辅酶Q10加200mcg硒,导致d -二聚体水平降低。D -二聚体水平反映血栓形成的可能性。在基线d-二聚体水平高于中位数的参与者中,在4.9年的随访期间,给予辅酶Q10加硒的参与者心血管死亡发生率较低17。在另一项对308名低硒老年人进行的为期四年的安慰剂对照试验中,CoQ10和硒的相同组合也被发现可以降低血管性血变因子和组织纤溶酶原激活物抑制剂-1的水平,这些分子在促进血栓形成中起关键作用18。在一项51名高LDL胆固醇水平受试者的随机对照试验中,与安慰剂相比,每天补充100或200mg辅酶Q10,连续8周可改善内皮功能,降低LDL氧化,增加一氧化氮可用性19。在一项随机安慰剂对照交叉试验中,36名患有抗磷脂综合征(一种与血栓形成风险增加相关的免疫疾病)的患者,每天200mg辅酶Q10持续一个月可改善血管功能;降低血栓风险、炎症和氧化应激标志物,以及29个动脉粥样硬化相关基因中有23个基因修饰表达20。
3. 维生素B族:
烟酸(维生素B3)是已知提高HDL胆固醇水平的更有效药物之一。HDL具有抗血栓作用,因为它能够保护内皮细胞免受氧化和其他损伤,并清除动脉壁上多余的胆固醇,防止可能导致血栓的斑块形成21。在他汀类药物开发之前,烟酸常用于治疗血脂异常。由于最近的证据表明,在他汀类药物治疗中添加缓释烟酸或提高HDL胆固醇水平对心血管结果几乎没有益处,因此烟酸不再被视为降低心血管风险的标准护理22-24。然而,烟酸已证明具有抗血栓作用,包括抑制一种名为因子VII的凝血级联酶,降低纤维蛋白原水平,降低组织因子的表达,抑制纤溶酶原激活物抑制物-1(一种抑制纤维蛋白溶解的酶),降低血液粘度,减少血小板聚集25。
叶酸、维生素B12和B6是同型半胱氨酸代谢所必需的,高血同水平与血管损伤和血栓形成风险增加有关。这些B族维生素,特别是叶酸和B12的低水平,以及高血同水平与动脉粥样硬化、中风和静脉血栓形成的风险增加有关26-28。例如,在心房颤动患者中,高同型蛋白(通常是由于B12缺乏)会使中风的风险增加四倍29。此外,恶性贫血,一种损害肠道B12吸收的疾病,与高同型半胱氨酸水平和静脉血栓形成风险升高有充分的联系30,31。
通过补充叶酸和B12减少高血同已被证明可以降低中风风险32。在一项随机对照试验中,10,789名患有高血压的中国成年人每天接受依那普利(一种降压药物)或依那普利与800 mcg叶酸的治疗,并随访4.2年。血小板数量低、同型半胱氨酸水平高的受试者中风风险最高,在这一高危亚组中,接受叶酸治疗的受试人中风风险低73%33。在另一项针对有DVT病史的中风患者的对照试验中,使用叶酸和B12降低高同型半胱氨酸浓度可将DVT复发率从28.9%降低到4.4%34。
4. 益生菌:
肠道微生物组与心血管健康之间的关系是一个深入研究的领域。越来越多的证据表明,微生态失调(微生物组组成失衡)是动脉粥样硬化和血栓形成的重要潜在因素35,36。
一项对15项随机对照试验(共976名参与者)的荟萃分析发现,补充乳杆菌,尤其是罗伊氏乳杆菌和植物乳杆菌,可以降低总胆固醇和LDL胆固醇水平,有助于降低心血管风险37。在一项针对127名高胆固醇水平受试者的随机安慰剂对照试验中,连续9周每天服用一种提供至少40亿CFU罗伊氏乳杆菌NCIMB 30242补充剂,可以降低LDL胆固醇水平,以及hs-CRP、载脂蛋白B-100(apoB-100)(一种与动脉粥样硬化发展相关的脂质成分)和纤维蛋白原水平38,39。同样,在一项包括114名高胆固醇患者的试验中,与安慰剂酸奶相比,一种含有14亿CFU罗伊氏乳杆菌NCIMB 30242的酸奶在六周内每天服用两次,降低了LDL胆固醇、apoB-100和非HDL胆固醇水平40。
其他益生菌菌株已被发现可以改善与血栓形成风险相关的参数。在一项对34名健康人进行的安慰剂对照试验中,连续12周每天饮用含有100亿CFU乳双歧杆菌和600mg精氨酸(一氧化氮的前体)的酸奶,可以改善血管功能,因此被认为可以降低动脉粥样硬化的风险41。一项对36名重度吸烟者进行的安慰剂对照试验发现,连续六周每天饮用200亿CFUs植物乳杆菌的饮料可以降低血压和纤维蛋白原水平,以及炎症细胞因子和氧化应激标志物的水平42。另一项针对32名人类免疫缺陷病毒(HIV)患者的试验比较了每日多菌株益生菌补充剂与安慰剂的效果,8周后,那些服用益生菌的人体内d -二聚体的水平下降幅度更大43。在小鼠中,摄入一种由产生溶栓酶纳豆激酶的枯草芽孢杆菌菌株发酵的奶制品可以减少血栓形成的发生44。
5. 维生素C:
维生素C是一种水溶性抗氧化剂,在实验室的高氧化应激促血栓形成条件下,已证明具有减少血小板聚集和促进纤维蛋白溶解的能力,而不会影响凝血途径45-47。特别是,维生素C似乎会降低内皮细胞和血小板粘附蛋白的表达46,48。一项对20,000多名年龄40-79岁的成年人的大规模研究,对这些人进行了平均9.5年的随访,发现血浆维生素C基线浓度最高的四分之一人群比最低四分之一人中风的风险低42%49。
一项对17项随机对照试验的荟萃分析发现,每天补充500至2000mg维生素C可以改善血管功能50,51。一些证据表明,补充维生素C可能会改善动脉粥样硬化和其他与静脉和动脉血栓风险增加相关的疾病,但这种影响可能是轻微的,对那些维生素C水平较低、心血管风险较高的人来说更为重要50,51。事实上,在连续四周每天两次服用1000mg维生素C后,对慢性心衰患者的血管扩张有积极影响52。
多项研究证明,吸烟者的血液中维生素C水平较低,每天口服2000mg维生素C可显著降低尿中异丙肾上腺素53、一种氧化应激标志物和单核细胞与血管内皮层的粘附,这是危险动脉粥样硬化斑块发展的早期阶段之一54。
6. 碧萝芷:
碧萝芷是一种来自法国海松树皮中的提取物,可预防长途飞行中引起的水肿和静脉血栓形成,并可能有助于慢性静脉不足55,56。在一项对照试验中,198名患有中高静脉血栓形成风险的航空乘客服用了碧萝芷,在长途飞行前和飞行期间服用200mg,第二天服用100mg,或服用安慰剂。安慰剂组有5例静脉血栓形成事件,碧萝芷组没有57。
在一项随机对照试验中,156名有单次DVT发作史的受试者中,150mg碧萝芷在一年后减少水肿方面与压缩袜一样有效,但由于压缩袜的不适,碧萝芷依从性更好58。在一项对222名有深静脉血栓病史的患者随访6年的观察性研究中,每天服用200mg碧萝芷的患者与服用血液稀释剂如阿司匹林、噻氯匹定(Ticlid)、舒洛地特(Aterina)或不服用药物的患者相比,深静脉血栓复发和血栓形成后综合征的风险更低59。碧萝芷还被发现通过增加健康受试者和冠状动脉疾病患者的一氧化氮生成来改善动脉内皮功能60,61。一个研究小组发现,连续两个月每天服用200mg碧萝芷可抑制慢性吸烟者因吸烟引起的血小板聚集升高,但对非吸烟者的血小板聚集没有影响62。
一项对307名有视网膜静脉血栓形成史的受试者进行的观察性研究发现,与阿司匹林、噻氯匹定、舒洛地特或不用药相比,每天服用100mg碧萝芷与复发性视网膜静脉血栓形成的发生率最低相关,并且是唯一与水肿减少相关的治疗方法63。一项类似设计的小型研究发现,与阿司匹林相比,9个月后,每天服用100mg碧萝芷与更好的视力、更低的视网膜水肿和复发性视网膜静脉血栓的风险以及更低的不良副作用发生率相关64。
7. 番茄红素:
番茄红素是一种类胡萝卜素,在番茄皮中含量很高。实验室和动物研究表明,番茄红素可能抑制组织因子活性并抑制血小板聚集65,66。番茄红素被认为可能通过减少内皮损伤、抑制LDL氧化、降低炎症免疫活性等机制预防血栓形成67。一项对28项观察性研究的荟萃分析发现,番茄红素的摄入量或血液水平越高,患中风和心血管疾病的风险越低68。
番茄加工副产品番茄渣含有番茄红素和多种番茄类黄酮,这些活性成分可以共同抑制血小板聚集并降低血栓形成风险69,70。在一项对99名健康年轻男性进行的安慰剂对照试验中,连续五天每天服用1000mg番茄渣提取物,可减少血小板聚集71。
8. 银杏叶:
银杏叶提取物可以刺激外周和冠状动脉循环,并可以预防神经和心血管疾病72-74。研究表明,银杏中的化合物可以减少氧化和炎症性内皮细胞损伤,改善血管功能,抑制动脉粥样硬化斑块的形成,并可能降低动脉血栓的风险75,76。
在一项涉及慢性静脉功能不全导致静脉血栓高风险患者的临床试验中,用银杏提取物治疗导致循环内皮细胞水平降低。循环内皮细胞被认为是血管持续损伤的标志77。证据还表明,银杏可以改善与血栓相关的疾病,包括高血压、不健康的血脂水平和高血糖水平78。
临床前研究表明,银杏提取物可抑制血小板活化因子(参与血小板活化),增加内皮细胞血栓调节蛋白的表达(激活凝血酶)和组织纤溶酶原激活物的产生(刺激纤维蛋白溶解)79,80。另有研究表明,银杏黄酮能直接抑制凝血酶活性81。然而,银杏似乎不会影响出血时间,使用银杏也不会增加出血的风险82,83。
9. 大蒜:
越来越多的研究表明,大蒜可以减缓动脉粥样硬化的进展,改善心脏代谢健康84。大蒜和大蒜提取物可以通过抑制血小板聚集、降低纤维蛋白原水平和增加纤溶过程来降低血栓形成风险85,86。一些证据表明,大蒜中的活性化合物Ajoene (阿霍烯)可能有助于其抗血栓特性87,88。
在一项临床试验中,36名健康的年轻男性每天接受600mg、1200mg或2400mg大蒜提取物或75mg血液稀释剂氯吡格雷,为期三周。接受1200mg或2400mg大蒜的患者的血液样本显示,对各种触发因素的反应,血小板聚集显著减少,并且剂量越高,效果越强。2400 mg剂量的大蒜在抑制血小板对某些但并非所有血栓触发因素的反应方面比氯吡格雷更有效。此外,所有参与者的出血时间都延长了(但保持在正常范围内),其中服用2400 mg大蒜提取物的参与者出血时间最长89。一项为期12周的安慰剂对照试验检查了陈蒜提取物与华法林治疗相结合的安全性。该试验包括48名密切监测的参与者,发现服用陈蒜提取物和华法林不会增加出血或其他不良副作用90。
10.橄榄油和橄榄叶:
特级初榨橄榄油(EVOO)富含单不饱和脂肪酸和抗氧化多酚,高摄入量一直与较低的心血管风险有关91。橄榄油已被证明可以降低氧化应激和炎症标志物水平,改善内皮功能以及脂质和碳水化合物代谢,并抑制血栓形成91,92。临床前研究表明,橄榄油可降低血小板活性和聚集,降低内皮细胞粘附分子的表达,降低凝血酶因子VII和纤溶酶原激活物抑制剂-1,这两者都与冠状动脉疾病有关93。一些证据表明,橄榄油可以减轻通常由高脂肪膳食引起的凝血酶活性的升高94。在一项针对82名早期动脉粥样硬化患者的临床试验中,每天30ml(1盎司)橄榄油,持续四个月,改善了血管功能和炎症标志物水平95。
橄榄多酚(Oleuropein)及其衍生物羟基酪醇(Hydroxytyrosol)是在橄榄、EVOO和橄榄叶中发现的多酚。这些化合物已显示出降低炎症和氧化应激的特性,并被发现可改善血管功能以及葡萄糖和脂质代谢96。多项临床前研究的结果表明,从EVOO和橄榄叶中提取的橄榄蛋白、羟基酪醇和其他酚类物质可抑制血小板活化和聚集97-99。
11.石榴:
石榴富含黄酮类化合物、单宁和其他多酚,具有较强的清除自由基和抗炎特性100。一项对八项随机对照试验的荟萃分析发现,每天饮用230ml石榴汁可以降低收缩压,每天饮用超过230ml石榴汁可以降低收缩和舒张压101。在一项针对13名健康受试者的公开试验中,连续两周每天饮用50ml(约两盎司)石榴汁,可使血小板聚集减少11%102。另一项临床试验发现,饮用石榴汁的受试者6小时后凝血时间延长103。
石榴还被发现可以减少氧化应激和高血压,并改善血管功能和糖脂代谢104,105。一项针对100名心脏病患者的随机安慰剂对照试验发现,每天450mg石榴提取物加180mg维生素E(dl-α-生育酚),持续8周,可降低两种血管粘附蛋白的表达,降低炎症标记物的水平106。另一项试验包括48名超重或肥胖的受试者,服用1000mg石榴提取物30天,可降低炎症标志物水平,改善血糖、胰岛素和LDL胆固醇水平107。
12.可可:
可可富含黄烷醇和其他多酚类物质,具有很强的自由基清除作用。研究发现,可可和黑巧克力可以降低血小板活化,抑制参与血小板聚集的蛋白质表达,并限制血小板活性对止血的影响108,109。可可除了含有多酚外,还含有可可碱(或咖啡碱),可可碱是甲基黄嘌呤家族中的一种化合物,也能抑制血小板聚集109。临床试验发现,可可中的多酚可以增加一氧化氮的产生,支持健康的内皮功能,降低炎症标志物水平,减少对脂质的氧化损伤,促进肠道有益细菌的生长110,111。
在健康男性的临床试验中,吃50g含有90%可可的巧克力,可以降低血小板反应性,延长四小时后采集的血液样本的凝血时间112,113。另一项临床试验发现,在健康男性中,食用黑巧克力可以抑制由实验性心理压力引起的d -二聚体水平的上升114。在一项针对健康中年人的开放标签对照试验中,每天900mg可可黄烷醇,持续30天,可改善内皮功能,这是血栓形成风险的一个重要因素;在后续的一项对照试验中,相同剂量也显示可改善血压和血脂水平115。
一项随机对照试验发现,在冠心病患者服用30天后,每天提供750mg黄烷醇的可可比低黄烷醇可可更能改善血管功能和内皮完整性标志物116。此外,富含黄烷醇的可可还被发现可以改善年轻的非裔美国人117、健康年轻群体118、绝经后妇女119、终末期肾病患者120、高血压男性121、健康的老年男性的血管功能122。
13. 绿茶:
绿茶被研究最多的是绿茶多酚(EGCG,表没食子儿茶素没食子酸酯)。临床试验和观察性研究发现,绿茶与降低心血管风险有关,因为它增加了一氧化氮的可用性,减少了炎症和氧化应激水平,改善了内皮功能123,124。
采用服用过血液稀释剂阿司匹林、氯吡格雷或替格瑞洛(Brilinta)的受试者血液样本进行的研究表明,EGCG可以在不增加出血风险的情况下改善其抗血小板作用125。EGCG已被证明可以抑制血小板中的炎症酶活性126,抑制炎症信号以及粘附分子的表达,促进内皮细胞中核因子红细胞2相关因子2 (Nrf2,一种上调抗氧化途径的蛋白)的表达123,127。EGCG还能抑制组织因子(一种触发动脉和静脉内皮细胞凝血的蛋白质)的表达128。
14. 槲皮素:
槲皮素是一种黄酮类化合物,存在于大多数水果和蔬菜中,在洋葱、苹果和葡萄酒中含量很高。黄酮类化合物(包括槲皮素)的摄入量越高,心血管风险越低129。研究发现,在健康成人中,补充150mg和300mg剂量的槲皮素可在30分钟内抑制血小板活化、信号传导和聚集130。在六周内补充150mg槲皮素也被证明可以显著降低收缩压和氧化LDL水平131。
临床前研究表明,槲皮素可以降低内皮细胞和血小板上粘附分子的表达,降低氧化应激,抑制LDL氧化,支持一氧化氮生成和健康血管功能,改善葡萄糖代谢,降低炎症标志物水平129,132。槲皮素和其他类黄酮被认为是蜂产品蜂胶和特种蜂蜜的抗血栓和心脏保护特性的原因133,134。
15. 生姜:
生姜是一种烹饪香料和草药,在临床上已证明具有心脏保护作用,如提高脂质水平、降低炎症细胞因子水平、降低血压和抑制血小板聚集135,136。一项观察性研究检查了4628名参与者的健康记录和饮食调查,发现在60岁及以上的人群中,那些报告较多使用生姜的人患冠状动脉疾病的几率较低137。生姜也可能对肥胖和2型糖尿病等代谢紊乱有益138。在一项对小鼠的研究中,姜酮(生姜的一种活性化合物)不仅抑制血小板聚集,还抑制因子Xa的活性,凝血过程中的一种酶139。实验室研究还发现,从生姜中提取的一种多糖抑制了凝血途径140。由于样本量小,使用的方法多变,对八项临床试验的系统综述无法就生姜对人类血小板聚集的影响得出确切结论141。在其中一项试验中,服用4g生姜三个月不会改变冠状动脉疾病患者的血小板聚集、纤维蛋白原水平或纤溶活性,但单次服用10g生姜会减少血小板聚集142。
16. 卡宴椒:
其所含辣椒素是一种活性化合物。辣椒素用于治疗炎症、代谢和感染性疾病143。临床前和临床证据表明,辣椒素可以改善脂质和葡萄糖代谢,支持减肥,并降低患2型糖尿病和心血管疾病的风险143-145。实验室证据表明,辣椒素有可能减少血小板聚集,而不影响凝血145,146。然而,在健康男性志愿者中,400 mcg和800 mcg的辣椒素都不影响血小板聚集147。
17. 姜黄素:
姜黄素是一种在烹饪香料姜黄中发现的类胡萝卜素,具有减少氧化应激和抗炎的特性。其潜在的抗血栓作用(包括抗血小板和抗凝)已在实验室和动物研究中得到证实148,149。一项临床前研究的结果表明,姜黄素可能有助于促进内皮修复和静脉血栓的解决150。在小鼠中,用姜黄素治疗可以防止炎症因子的增加,血压和暴露在空气污染(柴油废气)中的D-二聚体,这是一种已知会增加炎症和血栓风险的常见环境因素151。
18. 亚洲参:
在中国,三七提取物被静脉注射用于治疗急性血栓形成,一些证据表明,人参的口服提取物也可能具有抗血栓作用。生物活性皂苷,即人参皂苷,存在于中国人参、红参和西洋参中152-154。在一项为期28天的临床试验中发现了一种人参皂苷的口服制剂,可以减少血小板聚集155。
临床前研究表明,人参皂苷可以抑制血小板粘附分子的表达,血小板聚集和血小板对血栓触发物的反应性,这可能提供对过度血液凝结的保护156,157。此外,在实验室和动物研究中,人参皂苷已被证明可以减少血管炎症和僵硬,稳定动脉粥样硬化斑块,减缓动脉粥样硬化进展,这可能有助于预防血栓栓塞158。人参皂甙还可以通过减少自由基的产生、增加一氧化氮、增加血管内皮细胞的功能来改善血管功能,和调节脂质水平152。人参和人参皂苷具有抗炎和广泛的健康促进作用,可能有益于与血栓形成风险相关的个体152,159。人参中的其他化合物可能进一步促进其抗血小板活性160。
19. 马黛茶:
马黛茶富含抗炎和清除自由基特性的绿原酸161。在一项针对142名血液粘度高参与者的随机安慰剂对照试验中,6周内每天5g马黛茶可降低血液粘度,改善小血管的循环162。另一项对照临床试验发现,每天580mg马黛茶中的绿原酸可改善34名代谢综合征高危中年男性的心脏代谢健康标志物163。在临床前研究中,马黛茶的一种成分降低了凝血酶活化和静脉血栓形成164。
更多可点击其个性化的综合干预方案如下:
以及参阅本网如下专文的相关内容:
医疗干预
两类药物可降低血栓形成及其并发症风险,作为第三类的血栓溶解剂/纤维蛋白溶解剂(阿替普酶,tPA)一般用于医疗急救如脑梗塞、肺栓塞和心脏病发作等,可破坏血栓并减少组织损伤。
参考文献:
1. Golanski J et al. Effects of Omega-3 Polyunsaturated Fatty Acids and Their Metabolites on Haemostasis-Current Perspectives in Cardiovascular Disease. International journal of molecular sciences. Feb 27 2021;22(5)
2. Fan H et al. Meta-Analysis Comparing the Effect of Combined Omega-3 + Statin Therapy Versus Statin Therapy Alone on Coronary Artery Plaques. Am J Cardiol. 2021 Jul 15;151:15-24.
3. Bernasconi AA et al. Effect of Omega-3 Dosage on Cardiovascular Outcomes: An Updated Meta-Analysis and Meta-Regression of Interventional Trials. Mayo Clin Proc. Feb 2021;96(2):304-313.
4. Saber H et al. Omega-3 Fatty Acids and Incident Ischemic Stroke and Its Atherothrombotic and Cardioembolic Subtypes in 3 US Cohorts. Stroke. Oct 2017;48(10):2678-2685.
5. Lombardi M et al. Impact of Different Doses of Omega-3 Fatty Acids on Cardiovascular Outcomes: a Pairwise and Network Meta-analysis. Curr Atheroscler Rep. Jul 16 2020;22(9):45.
6. Zheng X et. Omega-3 fatty acids reduce post-operative risk of deep vein thrombosis and pulmonary embolism after surgery for elderly patients with proximal femoral fractures: a randomized placebo-controlled, double-blind clinical trial. Int Orthop. Oct 2020;44(10):2089-2093.
7. Viecelli AK et al. Fish oil and aspirin effects on arteriovenous fistula function: Secondary outcomes of the randomised omega-3 fatty acids (Fish oils) and Aspirin in Vascular access OUtcomes in REnal Disease (FAVOURED) trial. PLoS One. 2019;14(3):e0213274.
8. Isaksen T et al. Dietary intake of marine n-3 polyunsaturated fatty acids and future risk of venous thromboembolism. Research and practice in thrombosis and haemostasis. Jan 2019;3(1):59-69.
9. Isaksen T, Evensen LH, Brækkan SK, Hansen JB. Dietary Intake of Marine Polyunsaturated n-3 Fatty Acids and Risk of Recurrent Venous Thromboembolism. Thrombosis and haemostasis. Dec 2019;119(12):2053-2063.
10. Reiner MF et al. Omega-3 fatty acids predict recurrent venous thromboembolism or total mortality in elderly patients with acute venous thromboembolism. J Thromb Haemost. Jan 2017;15(1):47-56.
11. Shimizu M et al. Low coenzyme Q10 levels in patients with acute cardiovascular disease are associated with long-term mortality. Heart Vessels. Mar 2021;36(3):401-407.
12. Martelli A et al. Coenzyme Q(10): Clinical Applications in Cardiovascular Diseases. Antioxidants (Basel, Switzerland). Apr 22 2020;9(4)
13. Rabanal-Ruiz Y et al. The Use of Coenzyme Q10 in Cardiovascular Diseases. Antioxidants (Basel, Switzerland). May 10 2021;10(5)
14. Arenas-Jal M et al. Coenzyme Q10 supplementation: Efficacy, safety, and formulation challenges. Compr Rev Food Sci Food Saf. Mar 2020;19(2):574-594.
15. Ya F et al. Coenzyme Q10 Upregulates Platelet cAMP/PKA Pathway and Attenuates Integrin αIIbβ3 Signaling and Thrombus Growth. Mol Nutr Food Res. Dec 2019;63(23):e1900662.
16. Raizner AE et al. Coenzyme Q(10) for Patients With Cardiovascular Disease: JACC Focus Seminar. Journal of the American College of Cardiology. Feb 9 2021;77(5):609-619.
17. Alehagen U et al. Dietary Supplementation with Selenium and Coenzyme Q(10) Prevents Increase in Plasma D-Dimer While Lowering Cardiovascular Mortality in an Elderly Swedish Population. Nutrients. Apr 17 2021;13(4)
18. Alehagen U et al. Significant decrease of von Willebrand factor and plasminogen activator inhibitor-1 by providing supplementation with selenium and coenzyme Q10 to an elderly population with a low selenium status. European journal of nutrition. 2020/12/01 2020;59(8):3581-3590.
19. Sabbatinelli J et al. Ubiquinol Ameliorates Endothelial Dysfunction in Subjects with Mild-to-Moderate Dyslipidemia: A Randomized Clinical Trial. Nutrients. Apr 15 2020;12(4)
20. Pérez-Sánchez C et al. Ubiquinol Effects on Antiphospholipid Syndrome Prothrombotic Profile: A Randomized, Placebo-Controlled Trial. Arteriosclerosis, thrombosis, and vascular biology. Oct 2017;37(10):1923-1932.
21. Ramirez A et al. Low High-Density Lipoprotein and Risk of Myocardial Infarction. Clinical Medicine Insights Cardiology. 2015;9:113-7.
22. Subedi BH et al. Current guidelines for high-density lipoprotein cholesterol in therapy and future directions. Vasc Health Risk Manag. 2014;10:205-16. doi:10.2147/vhrm.S45648
23. Probstfield JL, Boden WE, Anderson T, et al. Cardiovascular outcomes during extended follow-up of the AIM-HIGH trial cohort. Journal of clinical lipidology. Nov-Dec 2018;12(6):1413-1419.
24. Landray MJ, Haynes R, Hopewell JC, et al. Effects of extended-release niacin with laropiprant in high-risk patients. The New England journal of medicine. Jul 17 2014;371(3):203-12.
25. Zeman M et al. Pleiotropic effects of niacin: Current possibilities for its clinical use. Acta pharmaceutica (Zagreb, Croatia). Dec 1 2016;66(4):449-469.
26. Zhou K et al. Association between B-group vitamins and venous thrombosis: systematic review and meta-analysis of epidemiological studies. Journal of thrombosis and thrombolysis. Nov 2012;34(4):459-67.
27. Zaric BL et al. Homocysteine and Hyperhomocysteinaemia. Curr Med Chem. 2019;26(16):2948-2961.
28. Amaral FM et al. Interactions among methylenetetrahydrofolate reductase (MTHFR) and cystathionine β-synthase (CBS) polymorphisms - a cross-sectional study: multiple heterozygosis as a risk factor for higher homocysteine levels and vaso-occlusive episodes. Genetics and molecular research Feb 23 2017;16(1)
29. Spence JD. Cardioembolic stroke: everything has changed. Stroke Vasc Neurol. Jun 2018;3(2):76-83.
30. Ammouri W et al. Venous thromboembolism and hyperhomocysteinemia as first manifestation of pernicious anemia: a case series. Journal of medical case reports. Sep 2 2017;11(1):250.
31. Prajapati K et al. Pernicious anaemia: cause of recurrent cerebral venous thrombosis. BMJ case reports. May 10 2021;14(5)
32. Spence JD. Homocysteine lowering for stroke prevention: Unravelling the complexity of the evidence. Int J Stroke. Oct 2016;11(7):744-7
33. Kong X et al. Platelet Count Affects Efficacy of Folic Acid in Preventing First Stroke. Journal of the American College of Cardiology. May 15 2018;71(19):2136-2146.
34. Shu XJ et al. Effects of folic acid combined with vitamin B12 on DVT in patients with homocysteine cerebral infarction. European review for medical and pharmacological sciences. May 2017;21(10):2538-2544.
35. Lässiger-Herfurth A et al. The Gut Microbiota in Cardiovascular Disease and Arterial Thrombosis. Microorganisms. Dec 13 2019;7(12)
36. Lippi G et al. The Intriguing Link between the Intestinal Microbiota and Cardiovascular Disease. Semin Thromb Hemost. Sep 2017;43(6):609-613.
37. Wu Y et al. Effect of probiotic Lactobacillus on lipid profile: A systematic review and meta-analysis of randomized, controlled trials. PLoS One. 2017;12(6):e0178868.
38. Jones ML et al. Cholesterol lowering and inhibition of sterol absorption by Lactobacillus reuteri NCIMB 30242: a randomized controlled trial. Eur J Clin Nutr. Nov 2012;66(11):1234-41.
39. Jones ML et al. Oral supplementation with probiotic L. reuteri NCIMB 30242 increases mean circulating 25-hydroxyvitamin D: a post hoc analysis of a randomized controlled trial. J Clin Endocrinol Metab. Jul 2013;98(7):2944-51. doi:10.1210/jc.2012-4262
40. Jones ML et al. Cholesterol-lowering efficacy of a microencapsulated bile salt hydrolase-active Lactobacillus reuteri NCIMB 30242 yoghurt formulation in hypercholesterolaemic adults. Br J Nutr. May 2012;107(10):1505-13.
41. Matsumoto M et al. Endothelial Function is improved by Inducing Microbial Polyamine Production in the Gut: A Randomized Placebo-Controlled Trial. Nutrients. May 27 2019;11(5)
42. Naruszewicz M et al. Effect of Lactobacillus plantarum 299v on cardiovascular disease risk factors in smokers. Am J Clin Nutr. Dec 2002;76(6):1249-55.
43. Stiksrud B et al. Reduced Levels of D-dimer and Changes in Gut Microbiota Composition After Probiotic Intervention in HIV-Infected Individuals on Stable ART. J Acquir Immune Defic Syndr. Dec 1 2015;70(4):329-37.
44. Zhang X et al. Screening of a Bacillus subtilis strain producing both nattokinase and milk-clotting enzyme and its application in fermented milk with thrombolytic activity. J Dairy Sci. Jul 1 2021;doi:10.3168/jds.2020-19756
45. Liu D et al. Effects and Mechanisms of Vitamin C Post-Conditioning on Platelet Activation after Hypoxia/Reoxygenation. Transfus Med Hemother. Apr 2020;47(2):110-118.
46. Tyml K. Vitamin C and Microvascular Dysfunction in Systemic Inflammation. Antioxidants (Basel, Switzerland). Jun 29 2017;6(3)
47. Mohammed BM et al. Impact of high dose vitamin C on platelet function. World journal of critical care medicine. Feb 4 2017;6(1):37-47.
48. Secor D et al. Ascorbate inhibits platelet-endothelial adhesion in an in-vitro model of sepsis via reduced endothelial surface P-selectin expression. Blood Coagul Fibrinolysis. Jan 2017;28(1):28-33.
49. Ashor AW et al. Effect of vitamin C and vitamin E supplementation on endothelial function: a systematic review and meta-analysis of randomized controlled trials. The British journal of nutrition. Apr 28 2015;113(8):1182-94.
50. Ashor AW et al. Limited evidence for a beneficial effect of vitamin C supplementation on biomarkers of cardiovascular diseases: an umbrella review of systematic reviews and meta-analyses. Nutr Res. Jan 2019;61:1-
51. Moser MA et al. Vitamin C and Heart Health: A Review Based on Findings from Epidemiologic Studies. International journal of molecular sciences. Aug 12 2016;17(8)
52. Hornig B et al. Vitamin C improves endothelial function of conduit arteries in patients with chronic heart failure. Circulation. Feb 3 1998;97(4):363-8.
53. Reilly M et al. Modulation of oxidant stress in vivo in chronic cigarette smokers. Circulation. Jul 1 1996;94(1):19-25.
54. Weber C et al. Increased adhesiveness of isolated monocytes to endothelium is prevented by vitamin C intake in smokers. Circulation. Apr 15 1996;93(8):1488-92.
55. Gulati OP. Pycnogenol® in chronic venous insufficiency and related venous disorders. Phytother Res. Mar 2014;28(3):348-62.
56. Belcaro G et al. Long-haul flights, edema, and thrombotic events: prevention with stockings and Pycnogenol® supplementation (LONFLIT Registry Study). Minerva cardioangiologica. Apr 2018;66(2):152-159.
57. Belcaro G et al. Prevention of venous thrombosis and thrombophlebitis in long-haul flights with pycnogenol. Clinical and applied thrombosis/hemostasis. Oct 2004;10(4):373-7.
58. Errichi BM et al. Prevention of post thrombotic syndrome with Pycnogenol® in a twelve month study. Panminerva medica. Sep 2011;53(3 Suppl 1):21-7.
59. Belcaro G et al. Prevention of recurrent venous thrombosis and post-thrombotic syndrome. Minerva cardioangiologica. Jun 2018;66(3):238-245.
60. Nishioka K et al. Pycnogenol, French maritime pine bark extract, augments endothelium-dependent vasodilation in humans. Hypertension research Sep 2007;30(9):775-80.
61. Enseleit F et al. Effects of Pycnogenol on endothelial function in patients with stable coronary artery disease: a double-blind, randomized, placebo-controlled, cross-over study. Eur Heart J. Jul 2012;33(13):1589-97.
62. Araghi-Niknam M et al. Pine bark extract reduces platelet aggregation. Integrative medicine . Mar 21 2000;2(2):73-77.
63. Belcaro G et al. Recurrent retinal vein thrombosis: prevention with Aspirin, Pycnogenol®, ticlopidine, or sulodexide. Minerva cardioangiologica. Apr 2019;67(2):109-114. doi:10.23736/s0026-4725.19.04891-6
64. Rodriguez P et al. Recurrence of retinal vein thrombosis with Pycnogenol® or Aspirin® supplementation: a registry study. Panminerva medica. Sep 2015;57(3):121-5.
65. Lee DK et al. Carotenoids enhance phosphorylation of Akt and suppress tissue factor activity in human endothelial cells. J Nutr Biochem. Nov 2006;17(11):780-6.
66. Sawardekar SB et al. Comparative evaluation of antiplatelet effect of lycopene with aspirin and the effect of their combination on platelet aggregation: An in vitro study. Indian journal of pharmacology. Jan-Feb 2016;48(1):26-31.
67. Thies F et al. Cardiovascular benefits of lycopene: fantasy or reality? The Proceedings of the Nutrition Society. May 2017;76(2):122-129.
68. Cheng HM et al. Lycopene and tomato and risk of cardiovascular diseases: A systematic review and meta-analysis of epidemiological evidence. Crit Rev Food Sci Nutr. 2019;59(1):141-158.
69. Concha-Meyer A et al. Platelet Anti-Aggregant Activity and Bioactive Compounds of Ultrasound-Assisted Extracts from Whole and Seedless Tomato Pomace. Foods. Oct 28 2020;9(11)
70. Fuentes E et al. Antiplatelet effects of bioactive compounds present in tomato pomace. Current drug targets. Jan 28 2021;
71. Palomo I et al. Chemical Characterization and Antiplatelet Potential of Bioactive Extract from Tomato Pomace (Byproduct of Tomato Paste). Nutrients. Feb 22 2019;11(2)
72. Zuo W et al. Advances in the Studies of Ginkgo Biloba Leaves Extract on Aging-Related Diseases. Aging Dis. Dec 2017;8(6):812-826.
73. Wu Y et al. Ginkgo biloba extract improves coronary blood flow in healthy elderly adults: role of endothelium-dependent vasodilation. Phytomedicine. Mar 2008;15(3):164-9.
74. Jung F et al. Effect of Ginkgo biloba on fluidity of blood and peripheral microcirculation in volunteers. Arzneimittel-Forschung. May 1990;40(5):589-93.
75. Sarkar C et al. Therapeutic promises of ginkgolide A: A literature-based review. Biomedicine & pharmacotherapy. Dec 2020;132:110908
76. Li X et al. New Insight into the Mechanisms of Ginkgo Biloba Extract in Vascular Aging Prevention. Curr Vasc Pharmacol. 2020;18(4):334-345.
77. Janssens D et al. Increase in circulating endothelial cells in patients with primary chronic venous insufficiency: protective effect of Ginkor Fort in a randomized double-blind, placebo-controlled clinical trial. Journal of cardiovascular pharmacology. Jan 1999;33(1):7-11.
78. Eisvand F et al. The effects of Ginkgo biloba on metabolic syndrome: A review. Phytother Res. Aug 2020;34(8):1798-1811.
79. Tian J et al. Ginkgo biloba Extract in Vascular Protection: Molecular Mechanisms and Clinical Applications. Curr Vasc Pharmacol. 2017;15(6):532-548.
80. Chiu YL et al. Ginkgo biloba Induces Thrombomodulin Expression and Tissue-Type Plasminogen Activator Secretion via the Activation of Krüppel-Like Factor 2 within Endothelial Cells. The American journal of Chinese medicine. 2020;48(2):357-372.
81. Chen TR et al. Biflavones from Ginkgo biloba as inhibitors of human thrombin. Bioorganic chemistry. Nov 2019;92:103199.
82. Kellermann AJ et al. Is there a risk of bleeding associated with standardized Ginkgo biloba extract therapy? A systematic review and meta-analysis. Pharmacotherapy. May 2011;31(5):490-502.
83. Ryu KH et al. Ginkgo biloba extract enhances antiplatelet and antithrombotic effects of cilostazol without prolongation of bleeding time. Thromb Res. Jul 2009;124(3):328-34.
84. Ansary J et al. Potential Health Benefit of Garlic Based on Human Intervention Studies: A Brief Overview. Antioxidants (Basel, Switzerland). Jul 15 2020;9(7)
85. Sobenin IA et al. Therapeutic effects of garlic in cardiovascular atherosclerotic disease. Chinese journal of natural medicines. Oct 2019;17(10):721-728.
86. Olas B. Anti-Aggregatory Potential of Selected Vegetables-Promising Dietary Components for the Prevention and Treatment of Cardiovascular Disease. Adv Nutr. Mar 1 2019;10(2):280-290.
87. Apitz-Castro R et al. A garlic derivative, ajoene, inhibits platelet deposition on severely damaged vessel wall in an in vivo porcine experimental model. Thromb Res. Aug 1 1994;75(3):243-9.
88. Apitz-Castro R et al. Effect of ajoene, the major antiplatelet compound from garlic, on platelet thrombus formation. Thromb Res. Oct 15 1992;68(2):145-55.
89. Fakhar H et al. Effect of the Garlic Pill in comparison with Plavix on Platelet Aggregation and Bleeding Time. Iran J Ped Hematol Oncol. 2012;2(4):146-52.
90. Macan H et al. Aged garlic extract may be safe for patients on warfarin therapy. J Nutr. Mar 2006;136(3 Suppl):793s-795s.
91. Katsiki N et al. Olive Oil Intake and Cardiovascular Disease Prevention: "Seek and You Shall Find". Current cardiology reports. May 7 2021;23(6):64.
92. Summerhill V et al. Vasculoprotective Role of Olive Oil Compounds via Modulation of Oxidative Stress in Atherosclerosis. Front Cardiovasc Med. 2018;5:188.
93. Cicerale S et al. Biological activities of phenolic compounds present in virgin olive oil. International journal of molecular sciences. Feb 2 2010;11(2):458-79.
94. Capurso C et al. Vascular effects of the Mediterranean diet part I: anti-hypertensive and anti-thrombotic effects. Vascul Pharmacol. Dec 2014;63(3):118-26.
95. Widmer RJ et al. Beneficial effects of polyphenol-rich olive oil in patients with early atherosclerosis. European journal of nutrition. Apr 2013;52(3):1223-31.
96. Peyrol J et al. Hydroxytyrosol in the Prevention of the Metabolic Syndrome and Related Disorders. Nutrients. Mar 20 2017;9(3)
97. Mizutani D et al. Olive polyphenol reduces the collagen-elicited release of phosphorylated HSP27 from human platelets. Bioscience, biotechnology, and biochemistry. Mar 2020;84(3):536-543.
98. Dell'Agli M et al. Inhibition of platelet aggregation by olive oil phenols via cAMP-phosphodiesterase. The British journal of nutrition. May 2008;99(5):945-51.
99. Singh I et al. The effects of polyphenols in olive leaves on platelet function. Nutr Metab Cardiovasc Dis. Feb 2008;18(2):127-32.
100. Fourati M et al. Bioactive Compounds and Pharmacological Potential of Pomegranate (Punica granatum) Seeds - A Review. Plant foods for human nutrition (Dordrecht, Netherlands). Dec 2020;75(4):477-486.
101. Sahebkar A et al. Effects of pomegranate juice on blood pressure: A systematic review and meta-analysis of randomized controlled trials. Pharmacological research : the official journal of the Italian Pharmacological Society . Jan 2017;115:149-161.
102. Aviram M et al. Pomegranate juice consumption reduces oxidative stress, atherogenic modifications to LDL, and platelet aggregation: studies in humans and in atherosclerotic apolipoprotein E-deficient mice. Am J Clin Nutr. May 2000;71(5):1062-76.
103. Polagruto JA et al. Effects of flavonoid-rich beverages on prostacyclin synthesis in humans and human aortic endothelial cells: association with ex vivo platelet function. Journal of medicinal food. Winter 2003;6(4):301-8.
104. Wang D et al. Vasculoprotective Effects of Pomegranate (Punica granatum L.). Front Pharmacol. 2018;9:544.
105. Delgado NTB et al. Protective Effects of Pomegranate in Endothelial Dysfunction. Curr Pharm Des. 2020;26(30):3684-3699.
106. Jafari T et al. Effects of pomegranate peel extract and vitamin E on the inflammatory status and endothelial function in hemodialysis patients: a randomized controlled clinical trial. Food Funct. Sep 23 2020;11(9):7987-7993.
107. Hosseini B et al. Effects of pomegranate extract supplementation on inflammation in overweight and obese individuals: A randomized controlled clinical trial. Complementary therapies in clinical practice. Feb 2016;22:44-50.
108. Magrone T et al. Cocoa and Dark Chocolate Polyphenols: From Biology to Clinical Applications. Front Immunol. 2017;8:677.
109. Aprotosoaie AC et al. The Cardiovascular Effects of Cocoa Polyphenols-An Overview. Diseases. Dec 17 2016;4(4)
110. Davinelli S et al. Short-term supplementation with flavanol-rich cocoa improves lipid profile, antioxidant status and positively influences the AA/EPA ratio in healthy subjects. J Nutr Biochem. Nov 2018;61:33-39.
111. Tzounis X et al. Prebiotic evaluation of cocoa-derived flavanols in healthy humans by using a randomized, controlled, double-blind, crossover intervention study. Am J Clin Nutr. Jan 2011;93(1):62-72.
112. Montagnana M et al. Dark chocolate modulates platelet function with a mechanism mediated by flavan-3-ol metabolites. Medicine. Dec 2018;97(49):e13432.
113. Montagnana M et al. Short-term effect of dark chocolate consumption on routine haemostasis testing. International journal of food sciences and nutrition. Aug 2017;68(5):613-616.
114. Von Känel R et al. Effects of dark chocolate consumption on the prothrombotic response to acute psychosocial stress in healthy men. Thrombosis and haemostasis. Dec 2014;112(6):1151-8.
115. Sansone R et al. Cocoa flavanol intake improves endothelial function and Framingham Risk Score in healthy men and women: a randomised, controlled, double-masked trial: the Flaviola Health Study. The British journal of nutrition. Oct 28 2015;114(8):1246-55.
116. Horn P et al. Dietary flavanol intervention lowers the levels of endothelial microparticles in coronary artery disease patients. The British journal of nutrition. Apr 14 2014;111(7):1245-52.
117. Kim K et al. Acute consumption of flavanol-rich cocoa beverage improves attenuated cutaneous microvascular function in healthy young African Americans. Microvascular research. Mar 2020;128:103931.
118. Pereira T et al. Randomized study of the effects of cocoa-rich chocolate on the ventricle-arterial coupling and vascular function of young, healthy adults. Nutrition (Burbank, Los Angeles County, Calif). Jul-Aug 2019;63-64:175-183.
119. Okamoto T, Kobayashi R, Natsume M, Nakazato K. Habitual cocoa intake reduces arterial stiffness in postmenopausal women regardless of intake frequency: a randomized parallel-group study. Clin Interv Aging. 2016;11:1645-1652.
120. Rassaf T et al. Vasculoprotective Effects of Dietary Cocoa Flavanols in Patients on Hemodialysis: A Double-Blind, Randomized, Placebo-Controlled Trial. Clinical journal of the American Society of Nephrology : CJASN. Jan 7 2016;11(1):108-18.
121. Rull G et al. Effects of high flavanol dark chocolate on cardiovascular function and platelet aggregation. Vascul Pharmacol. Aug 2015;71:70-8.
122. Heiss C et al. Impact of cocoa flavanol intake on age-dependent vascular stiffness in healthy men: a randomized, controlled, double-masked trial. Age (Dordr). Jun 2015;37(3):9794.
123. Yamagata K. Protective Effect of Epigallocatechin Gallate on Endothelial Disorders in Atherosclerosis. Journal of cardiovascular pharmacology. Apr 2020;75(4):292-298.
124. Slevin M et al. Unique vascular protective properties of natural products: supplements or future main-line drugs with significant anti-atherosclerotic potential? Vasc Cell. Apr 30 2012;4(1):9.
125. Joo HJ et al. Anti-platelet effects of epigallocatechin-3-gallate in addition to the concomitant aspirin, clopidogrel or ticagrelor treatment. The Korean journal of internal medicine. May 2018;33(3):522-531.
126. Lee DH et al. Inhibitory effects of epigallocatechin-3-gallate on microsomal cyclooxygenase-1 activity in platelets. Biomolecules & therapeutics. Jan 2013;21(1):54-9.
127. Reddy AT et al. Epigallocatechin gallate suppresses inflammation in human coronary artery endothelial cells by inhibiting NF-κB. Life Sci. Oct 1 2020;258:118136.
128. Zhang Z et al. Potential protective mechanisms of green tea polyphenol EGCG against COVID-19. Trends Food Sci Technol. Aug 2021;114:11-24.
129. Anand David AV et al. Overviews of Biological Importance of Quercetin: A Bioactive Flavonoid. Pharmacogn Rev. Jul-Dec 2016;10(20):84-89.
130. Hubbard GP et al. Ingestion of quercetin inhibits platelet aggregation and essential components of the collagen-stimulated platelet activation pathway in humans. J Thromb Haemost. Dec 2004;2(12):2138-45.
131. Egert S et al. Quercetin reduces systolic blood pressure and plasma oxidized low-density lipoprotein concentrations in overweight subjects with a high-cardiovascular disease risk phenotype: a double-blinded, placebo-controlled cross-over study. The British journal of nutrition. Oct 2009;102(7):1065-74.
132. Patel RV et al. Therapeutic potential of quercetin as a cardiovascular agent. European journal of medicinal chemistry. Jul 15 2018;155:889-904.
133. Zhang YX et al. Inhibitory Effect of Propolis on Platelet Aggregation In Vitro. J Healthc Eng. 2017;2017:3050895.
134. Olas B. Honey and Its Phenolic Compounds as an Effective Natural Medicine for Cardiovascular Diseases in Humans? Nutrients. Jan 21 2020;12(2)doi:10.3390/nu12020283
135. Li C et al. Vasculoprotective effects of ginger (Zingiber officinale Roscoe) and underlying molecular mechanisms. Food Funct . Mar 15 2021;12(5):1897-1913.
136. Fakhri S et al. Ginger and Heart Health: From Mechanisms to Therapeutics. Current molecular pharmacology. 2021;14(6):943-959.
137. Wang Y et al. Evaluation of daily ginger consumption for the prevention of chronic diseases in adults: A cross-sectional study. Nutrition (Burbank, Los Angeles County, Calif). Apr 2017;36:79-84.
138. Mao QQ et al. Bioactive Compounds and Bioactivities of Ginger (Zingiber officinale Roscoe). Foods. May 30 2019;8(6)
139. Lee W et al. Anti-factor Xa activities of zingerone with anti-platelet aggregation activity. Food and chemical toxicology Jul 2017;105:186-193.
140. Wang C et al. Sulfation, structural analysis, and anticoagulant bioactivity of ginger polysaccharides. Journal of food science. Aug 2020;85(8):2427-2434.
141. Marx W et al. The Effect of Ginger (Zingiber officinale) on Platelet Aggregation: A Systematic Literature Review. PLoS One. 2015;10(10):e0141119.
142. Bordia A et al. Effect of ginger (Zingiber officinale Rosc.) and fenugreek (Trigonella foenumgraecum L.) on blood lipids, blood sugar and platelet aggregation in patients with coronary artery disease. Prostaglandins Leukot Essent Fatty Acids. May 1997;56(5):379-84.
143. Sanati S et al. A review of the effects of Capsicum annuum L. and its constituent, capsaicin, in metabolic syndrome. Iranian journal of basic medical sciences. May 2018;21(5):439-448.
144. Panchal SK et al. Capsaicin in Metabolic Syndrome. Nutrients. May 17 2018;10(5)
145. Fattori V et al. Capsaicin: Current Understanding of Its Mechanisms and Therapy of Pain and Other Pre-Clinical and Clinical Uses. Molecules (Basel, Switzerland). Jun 28 2016;21(7)
146. Almaghrabi S et al. Synergistic inhibitory effect of capsaicin and dihydrocapsaicin on in-vitro platelet aggregation and thromboxane formation. Blood Coagul Fibrinolysis. Jun 2018;29(4):351-355.
147. Sandor B et al. Orally given gastroprotective capsaicin does not modify aspirin-induced platelet aggregation in healthy male volunteers (human phase I examination). Acta physiologica Hungarica. Dec 2014;101(4):429-37.
148. Keihanian F et al. Curcumin, hemostasis, thrombosis, and coagulation. J Cell Physiol. Jun 2018;233(6):4497-4511.
149. Tabeshpour J et al. The regulatory role of curcumin on platelet functions. Journal of cellular biochemistry. Nov 2018;119(11):8713-8722.
150. Wang T et al Curcumin promotes venous thrombi resolve process in a mouse deep venous thrombosis model via regulating miR-499. Microvascular research. Jul 2021;136:104148.
151. Nemmar A et al. Protective effect of curcumin on pulmonary and cardiovascular effects induced by repeated exposure to diesel exhaust particles in mice. PLoS One. 2012;7(6):e39554.
152. Ratan ZA et al. Pharmacological potential of ginseng and its major component ginsenosides. J Ginseng Res. Mar 2021;45(2):199-210.
153. Luo BY et al. The effects of ginsenosides on platelet aggregation and vascular intima in the treatment of cardiovascular diseases: From molecular mechanisms to clinical applications. Pharmacological research. Sep 2020;159:105031.
154. Wang MM et al. Panax quinquefolium saponin combined with dual antiplatelet drugs inhibits platelet adhesion to injured HUVECs via PI3K/AKT and COX pathways. Journal of ethnopharmacology. Nov 4 2016;192:10-19.
155. Wang J et al. [Effect of Radix notoginseng saponins on platelet activating molecule expression and aggregation in patients with blood hyperviscosity syndrome]. Zhongguo Zhong xi yi jie he. Apr 2004;24(4):312-6.
156. Zuo X et al. Ginsenosides Rb2 and Rd2 isolated from Panax notoginseng flowers attenuate platelet function through P2Y(12)-mediated cAMP/PKA and PI3K/Akt/Erk1/2 signaling. Food Funct. 2021 Jul 5;12(13):5793-5805.
157. Xu ZY, Xu Y, Xie XF, et al. Anti-platelet aggregation of Panax notoginseng triol saponins by regulating GP1BA for ischemic stroke therapy. Chinese medicine. Jan 19 2021;16(1):12. doi:10.1186/s13020-021-00424-3
158. Xue Q et al. Functional roles and mechanisms of ginsenosides from Panax ginseng in atherosclerosis. J Ginseng Res. Jan 2021;45(1):22-31.
159. Yoon SJ et al. Effect of Korean Red Ginseng on metabolic syndrome. J Ginseng Res. May 2021;45(3):380-389.
160. Irfan M et al. Gintonin modulates platelet function and inhibits thrombus formation via impaired glycoprotein VI signaling. Platelets. 2019;30(5):589-598.
161. Lutomski P et al. Health properties of Yerba Mate. Ann Agric Environ Med. Jun 19 2020;27(2):310-313.
162. Yu S et al. Yerba mate (Ilex paraguariensis) improves microcirculation of volunteers with high blood viscosity: a randomized, double-blind, placebo-controlled trial. Exp Gerontol. Feb 2015;62:14-22.
163. Gebara KS, Gasparotto Junior A, Palozi RAC, et al. A Randomized Crossover Intervention Study on the Effect a Standardized Maté Extract (Ilex paraguariensis A. St.-Hil.) in Men Predisposed to Cardiovascular Risk. Nutrients. Dec 23 2020;13(1)
164. Dahmer T, Berger M, Barlette AG, et al. Antithrombotic effect of chikusetsusaponin IVa isolated from Ilex paraguariensis (Maté). Journal of medicinal food. Dec 2012;15(12):1073-80.
参考来源:
美国梅奥诊所
www.mayoclinic.org
美国血栓病学会
www.bloodclot.org
美国医疗在线网
www.webmd.com
美国卒中协会
http://www.stroke.org
加拿大心脏和卒中基金会
http://www.heartandstroke.com
免责声明和安全信息
英文名称:Blood Clots Prevention,Thrombosis,Thrombotic Disease
定义
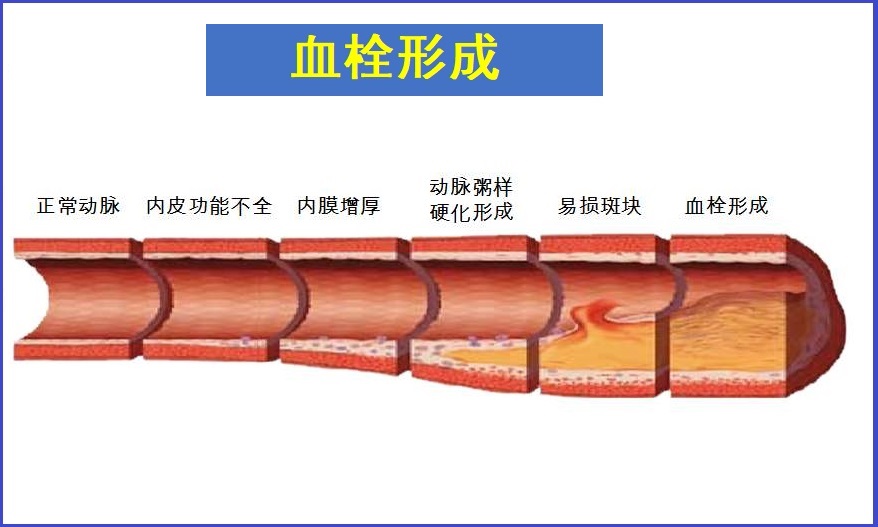
血栓病是血管内形成异常的血凝块而造成的疾病。血栓形成与血管受损、血液改变和血流淤滞有关。血栓病是许多慢性疾病的基础病因,如冠心病、心肌梗塞、脑梗塞和肺栓塞等。血栓一般由血凝块发展而来,血凝块由血小板、红细胞、白血细胞和纤维蛋白组成。根据来源,血栓可分为:
- 血栓形成:因多种因素在血管内逐步形成直到影响或阻止血流,特点是静止不动。例如脑血栓(脑血栓形成)、心肌梗塞(心脏病发作)。
- 栓塞:血凝块破裂成更多小凝块后在血液中循环,小血凝块进入较小的动静脉时可能引起堵塞或栓塞,这种小血凝块就称为栓子,典型例子如脑栓塞、肺栓塞。
根据血栓形成的部位,血栓又可分为动脉血栓、静脉血栓:
- 动脉血栓,主要是由血小板和纤维蛋白组成,通常发生在血流较快而血管壁有损伤或异常部位。常见如冠状动脉疾病(冠心病)、颈动脉疾病(脑梗塞)、外周动脉疾病(下肢动脉闭塞症)等。
- 静脉血栓,通常由血流缓慢或淤滞所引起,特点是含有大量红细胞和纤维蛋白。常见如:浅静脉血栓形成,深静脉血栓形成(DVT)和肺栓塞(PE)。
病因与风险因素
当血管创伤、血流停滞等发生时就可引起凝血(止血)和血栓,血栓来自于血凝块。血凝是生命活动不可或缺的组成部分,没有血凝就不能止血,而异常的血凝导致的血栓形成,将严重影响心脑血管健康。血栓形成及影响因素主要通过如下三种机制中的一种或多种产生:
- 改变或损害血管内皮:血管内皮的改变产生不一定是撕裂的干扰区域,但仍然可以模仿血管损伤的生理学,从而促进血小板的募集和凝血过程。影响内皮细胞健康的因素包括:
- 血脂异常:尤其是总胆固醇升高、“坏”胆固醇,高甘油三酯和低水平“好”胆固醇,对内皮细胞健康构成威胁。
- 高致敏性C-反应蛋白(CRP):这是炎症和血管损伤的指标,高水平可预测未来心脏病发作或中风的风险。 CRP还发挥几种促血栓形成活性,并可能与静脉血栓形成的风险相关。
- 高血压:持续的高血压会损害内皮的完整性,并可导致内皮细胞活化和凝血的开始。为了获得最佳的内皮保护和血栓预防,建议目标血压值为115/75 mmHg。
- 高血糖:高血糖水平可诱导血小板聚集。
- 腹部脂肪过多:腹部脂肪容易分泌炎症化学物并导致高血糖和高血压,这些因素都对内皮细胞的健康构成严重威胁。
- 高同型半胱氨酸血症:与静脉血栓形成风险增加60%相关。同型半胱氨酸损害内皮,增加内皮细胞和血小板活化,并降低纤维蛋白溶解活性
- 既往心脑血管病史,如中风、短暂性脑缺血发作、心脏病发作或冠心病均表明对动脉血栓形成的易感性,是未来血栓形成事件的最强预测因子。
- 阻扰或减缓血液流动:可通过循环血小板和凝血因子的局部积累并通过增加凝血反应来刺激血栓形成。这些风险因素包括:
- 缺乏身体活动,或久坐不动的生活方式。
- 下肢(臀部、膝盖、踝部)的躯干会增加血栓形成的风险,这可能与手术引起的静脉损伤或恢复期间的固定有关。
- 心房颤动:最常见的心律失常,可导致心脏血液汇集,并导致左心房血栓形成,使卒中风险增加5倍。
- 促进有利于过度凝固(高凝)的状态:血液性质或组成促进凝血的条件,有些是遗传因素,更常见的非遗传高凝状态因素,包括:
- 甲状腺疾病(甲亢、甲减):可改变凝血因子和抗凝血剂的平衡,并可增加血栓形成的风险。
- 高血浆纤维蛋白原:一种主要的凝血蛋白,可能由多种疾病引起,如吸烟、甲状腺疾病或感染等。
- 妊娠,尤其是先兆子痫。
- 癌症:可使静脉血栓形成的风险增加4至7倍,特别是在转移性癌症或肿瘤浸润或血管压迫破坏血流的情况下。血凝块也可预测癌症风险。肿瘤对血液发挥许多促血栓形成作用,化疗本身也是如此。不幸的是,一旦癌症进展到足以导致血液凝块,它通常处于晚期阶段。
- 手术:可增加血栓形成的风险
- 其他风险因素,包括年龄、女性、吸烟和肥胖等。
凝血机制与干预
凝血是止血所必须的,止血是生命活动的基础,包括修复大血管损伤,以及每日数以千计的微观撕裂。没有适当的止血反应,最小的血管损伤都能导致危及生命的出血。正常的凝血过程是一系列化学相互作用结果,主要包括血管收缩、血小板栓塞形成阻塞、凝血反应,形成凝块密封孔直到组织修复发生。当受损组织愈合时,不需要的血凝块—坚韧的纤维蛋白链溶解,血液回收凝块的血小板和血细胞。
凝血机制和可干预措施包括如下:
1.血管损伤与收缩:
当血管内皮发生损伤,血管收缩及其附近部位血流减少以利于凝血反应。例如动脉粥样硬化斑块破裂或高同型半胱氨酸所致的内皮损伤。
- 保护血管内皮细胞免受损伤、维持血管弹性是介导的有效途径。研究表明,多酚类物质有此类预防作用,包括原花青素(葡萄籽)、白藜芦醇等。
2.血小板粘附和活化:血小板活化后在血小板之间自我传播、粘附,并靠近在血管壁损伤部位附近。
当循环血小板经过血管壁损伤部位时,则在其周围粘附和结合,这种结合导致血小板活化并可募集更多的血小板。
- 药物干预:阿司匹林、氯吡格雷可抑制血小板粘附,或缩短其寿命期。
- 自然物质干预:姜黄素、大蒜提取物和鱼油等可抑制血小板粘附、降低其活化。
血小板聚集与可干预路径:血小板激活或活化后,其表面受体可绑定纤维蛋白原形成凝块(约占总血液蛋白4%)。
自然物质干预路径如:
- 烟酸,可降低血浆纤维蛋白原水平,弱化血小板聚集血凝作用。
- 维生素C,能降低血浆纤维蛋白原水平。
- 番茄红素,可阻止血小板受体绑定纤维蛋白原。
- 橄榄油,可升高血浆的一种载脂蛋白水平,降低血小板受体功能,抑制积聚。
4.凝血反应:纤维蛋白凝胶和血细胞和血小板随后与血小板栓塞融合以加强损伤并完全密封它直到组织修复开始。
4.1.凝血反应过程与可干预路径:在血小板栓塞形成同时,在血管壁损伤时释放的组织因子和胶原蛋白引发两个(内源和外源)的独立但相关的凝血途径,产生更多的凝血酶以转化纤维蛋白:
- 胶原与因子XII相互作用以启动内源性凝血级联反应;组织因子与因子VII相互作用以启动外源性凝血级联反应。
- 内源和外源2个凝血途径汇聚到一起,通过一系列复杂的相互作用,将凝血酶原(因子II)转化为凝血酶,并自我繁殖转化更多凝血酶原。
- 然后,凝血酶作用于循环纤维蛋白原将其转化为纤维蛋白。
- 干预I—肝素:肝素是一种天然抗凝剂,可增强抗凝血酶的作用,以抑制纤维蛋白生成,从而减缓凝血过程。肝素治疗在心房颤动和深静脉血栓形成(DVT)的医疗急救期使用是有帮助的。
- 干预II—达比加群:凝血酶抑制剂,可直接抑制凝血酶的作用,阻止其将纤维蛋白原转化为纤维蛋白。
- 单个纤维蛋白颗粒彼此结合形成聚合物,聚合物结合成网状凝胶,其捕获循环的白细胞、红细胞和额外的血小板组成血凝块(血栓)。
- 干预—华法林:通过抑制维生素K活性,沿内源和外源的凝血途径干扰凝血过程。
- 维生素K是激活参与凝血的许多因子(II、VII、IX、X等)所必须的,华法林抑制维生素K还原及阻止其再循环利用,从而减缓凝血所需因子的活化。
4.2.纤维蛋白溶解(纤溶):
在血凝完成后(通常在损伤后3-6分钟),凝块内被捕获的血小板开始缩回,凝块收缩更靠近伤口边缘,挤出任何多余的凝血因子。然后,开始修理损伤。一旦愈合,通过纤维蛋白溶解(纤溶)过程溶解并除去不需要的凝块。
- 纤溶涉及纤溶酶对纤维蛋白网的切割,以释放被捕获的血细胞和血小板,使凝块“溶解”。
- 一种组织纤溶酶原激活剂(tPA,又称阿替普酶)的酶将无活性蛋白质纤溶酶原转化为活性纤溶酶,然后切割纤维蛋白网。
- 药物干预:在涉及栓塞发作的医疗紧急事件中,如栓塞性中风、肺栓塞和心肌梗塞),tPA可静脉注射以溶解血凝块并改善临床结果。 tPA应在栓塞事件后尽快给予,以获得最大利益。
- 自然干预:纳豆激酶是一种来自日本大豆的发酵产物,已被证明能增加血浆纤维蛋白溶解活性的酶。
症状
血栓病症状因不同类型血栓而不同,具体如下:- 动脉血栓:早期可能没有症状,随着血凝块增长或阻塞更多血流,可能出现如下:
- 手臂、腿脚发冷、冰凉
- 受影响区域的肌肉痉挛或疼痛不适
- 手臂、腿部麻木、刺痛
- 肢体端苍白、无色
- 肢体无力、弱化
- 静脉血栓症状,可包括如下:
浅静脉血栓症状如:
- 皮肤疼痛、肿胀和发炎
- 触感柔软、疼痛
- 皮肤发红、红肿
深静脉血栓(DVT)症状包括:
- 单腿或双腿肿胀
- 受影响的腿疼痛、或沉重感
- 小腿痉挛性疼痛,弯曲时可能会更糟
- 血栓附近的皮肤温热、发红
注意:DVT是一种医疗急症,如果出现上述症状,应立即就医,以免产生可能危及生命的并发症(肺栓塞、呼吸困难和胸部疼痛)。
并发症
血栓形成可导致的并发症包括如下:- 动脉血栓形成引起的并发症如:
- 脑卒中/中风:由血栓引起的缓慢发展,或由栓塞引起的快速发作。
- 短暂性脑缺血发作(TIA)。
- 心肌梗死(心脏病发作):阻塞向心肌供氧的冠状动脉。
- 肺栓塞:危及生命的肺部动脉堵塞,使体内的氧气不足,这是常见的危及生命的并发症。导致肺栓塞的血凝块通常在腿部形成深静脉血栓(DVT),但也可在心房纤颤患者的心房中形成。
- 心绞痛:心脏血液供应减少,通常导致严重的胸痛。
- 由静脉血栓形成引起的并发症如:
- 深静脉血栓形成(DVT):通常在腿部,且很普遍。由DVT形成的不稳定凝块(栓子)有可能脱离并移动到为肺部提供脱氧血液的动脉,在那里它们可能导致潜在致命的肺栓塞。 DVT的损伤也可导致血栓后综合征,这是一种以腿痛、沉重、肿胀或溃疡为代表的病症。超过三分之一的DVT女性患有血栓后综合征。
- 门静脉血栓形成:一种罕见的静脉阻塞,将血液从腹部运送到肝脏。门静脉血栓形成相对罕见,通常与肝脏疾病有关。
- 肾静脉血栓形成:从肾脏排出血液的静脉阻塞。这种类型的血栓形成相对罕见,并且通常与腹部创伤有关。
疗法
综合选项包括如下:调整饮食与生活方式
导致血栓病的原因和风险因素,主要包括高胆固醇、高血压、糖尿病和动脉粥样硬化,以及高同型半胱氨酸血症等,了解更多可点击本网的相关专文内容。
营养与草本综合干预
以下是基于循证医学和循证营养学有关文献综合的结果。
有助于防控血栓病的营养和草本补充剂,主要包括如下:
1.鱼油:
EPA和DHA通过调节血小板和内皮功能来影响止血和血栓形成。EPA和DHA已被证明可降低血小板反应性和聚集性,增加一氧化氮的产生,抑制氧化LDL的产生,并降低内皮细胞表面粘附分子的表达。它们还可以通过减少组织因子的表达来促进纤维蛋白溶解并抑制凝血级联反应1。
一项对八项随机对照试验数据的荟萃分析发现,在稳定和促进冠状动脉动脉粥样硬化斑块消退方面,ω-3脂肪酸联合他汀类药物治疗比单独他汀类药物更有效,可能降低动脉血栓栓塞的风险2。另一项对40项随机对照试验的荟萃分析发现,补充EPA和DHA可降低心脏病发作和心血管死亡的风险,共有135,267名参与者。分析进一步计算出,每天每多摄入1g 的EPA和DHA,心血管事件的风险就会降低5.8%3。
一项利用三项大型队列研究的观察性证据进行的研究表明,血液中DHA水平越高,患动脉粥样硬化性血栓性中风的风险越低,而血液中二十二碳五烯酸(DPA)水平越高则患心脏栓塞性中风(因冠状动脉栓塞引起)的危险越低4。DPA是鱼类中发现的另一种ω-3脂肪酸;它可以在体内由EPA制成,并进一步转化为DHA。
然而,一项对125,763名受试者进行的14项试验的荟萃分析发现,尽管这些试验与心脏病发作和其他主要心血管事件的风险较低有关,但摄入1g或更多的ω-3脂肪酸与出血和发生心房颤动的风险增加有关5。对于有心房颤动病史或有高风险的人,建议谨慎使用鱼油,或遵循医生指导。
一项随机、对照试验对452名因骨折需要腿部手术的老年人进行了研究,发现术后30天服用1g 欧米伽-3脂肪酸可降低深静脉血栓和肺栓塞的风险,且不会增加出血事件或其他并发症6。在567例慢性肾病患者中,连续3个月每天服用4g omega-3脂肪酸可降低用于透析的动静脉瘘急性血栓形成的风险7。一项针对21,970名参与者的观察性研究发现,在中位随访11.6年后,每周从饮食和补充剂中摄入超过4.7g的鱼类omega-3脂肪酸与静脉血栓栓塞风险降低22-26%和肺栓塞风险降低39-60%相关8。较高的omega-3脂肪酸摄入量也与较低的DVT复发率或其他静脉血栓栓塞事件相关,特别是对于那些首次事件没有已知诱因的患者(如手术、住院、癌症或急性疾病)9,10。
2. 辅酶Q10:
辅酶Q10(CoQ10)是一种参与线粒体中还原-氧化平衡和能量产生的营养物质。低CoQ10水平可增加炎症信号传导,并与不良的心血管健康和结果有关,CoQ10补充剂在预防和辅助治疗心血管疾病和相关代谢状况方面具有潜在作用11-14。CoQ10已被发现通过减少动脉壁中氧化的LDL积累来改善血管功能,减少血管损伤和僵硬,增加一氧化氮的可用性13。实验室研究进一步表明,辅酶Q10可以抑制血小板聚集和信号传导,减少血栓生长15。因为使用他汀类药物可降低辅酶Q10的产生,服用他汀类药物的患者尤其可以从补充辅酶Q10中受益14,16。
在一项随机对照试验中,213名低硒老年人连续四年服用200mg辅酶Q10加200mcg硒,导致d -二聚体水平降低。D -二聚体水平反映血栓形成的可能性。在基线d-二聚体水平高于中位数的参与者中,在4.9年的随访期间,给予辅酶Q10加硒的参与者心血管死亡发生率较低17。在另一项对308名低硒老年人进行的为期四年的安慰剂对照试验中,CoQ10和硒的相同组合也被发现可以降低血管性血变因子和组织纤溶酶原激活物抑制剂-1的水平,这些分子在促进血栓形成中起关键作用18。在一项51名高LDL胆固醇水平受试者的随机对照试验中,与安慰剂相比,每天补充100或200mg辅酶Q10,连续8周可改善内皮功能,降低LDL氧化,增加一氧化氮可用性19。在一项随机安慰剂对照交叉试验中,36名患有抗磷脂综合征(一种与血栓形成风险增加相关的免疫疾病)的患者,每天200mg辅酶Q10持续一个月可改善血管功能;降低血栓风险、炎症和氧化应激标志物,以及29个动脉粥样硬化相关基因中有23个基因修饰表达20。
3. 维生素B族:
烟酸(维生素B3)是已知提高HDL胆固醇水平的更有效药物之一。HDL具有抗血栓作用,因为它能够保护内皮细胞免受氧化和其他损伤,并清除动脉壁上多余的胆固醇,防止可能导致血栓的斑块形成21。在他汀类药物开发之前,烟酸常用于治疗血脂异常。由于最近的证据表明,在他汀类药物治疗中添加缓释烟酸或提高HDL胆固醇水平对心血管结果几乎没有益处,因此烟酸不再被视为降低心血管风险的标准护理22-24。然而,烟酸已证明具有抗血栓作用,包括抑制一种名为因子VII的凝血级联酶,降低纤维蛋白原水平,降低组织因子的表达,抑制纤溶酶原激活物抑制物-1(一种抑制纤维蛋白溶解的酶),降低血液粘度,减少血小板聚集25。
叶酸、维生素B12和B6是同型半胱氨酸代谢所必需的,高血同水平与血管损伤和血栓形成风险增加有关。这些B族维生素,特别是叶酸和B12的低水平,以及高血同水平与动脉粥样硬化、中风和静脉血栓形成的风险增加有关26-28。例如,在心房颤动患者中,高同型蛋白(通常是由于B12缺乏)会使中风的风险增加四倍29。此外,恶性贫血,一种损害肠道B12吸收的疾病,与高同型半胱氨酸水平和静脉血栓形成风险升高有充分的联系30,31。
通过补充叶酸和B12减少高血同已被证明可以降低中风风险32。在一项随机对照试验中,10,789名患有高血压的中国成年人每天接受依那普利(一种降压药物)或依那普利与800 mcg叶酸的治疗,并随访4.2年。血小板数量低、同型半胱氨酸水平高的受试者中风风险最高,在这一高危亚组中,接受叶酸治疗的受试人中风风险低73%33。在另一项针对有DVT病史的中风患者的对照试验中,使用叶酸和B12降低高同型半胱氨酸浓度可将DVT复发率从28.9%降低到4.4%34。
4. 益生菌:
肠道微生物组与心血管健康之间的关系是一个深入研究的领域。越来越多的证据表明,微生态失调(微生物组组成失衡)是动脉粥样硬化和血栓形成的重要潜在因素35,36。
一项对15项随机对照试验(共976名参与者)的荟萃分析发现,补充乳杆菌,尤其是罗伊氏乳杆菌和植物乳杆菌,可以降低总胆固醇和LDL胆固醇水平,有助于降低心血管风险37。在一项针对127名高胆固醇水平受试者的随机安慰剂对照试验中,连续9周每天服用一种提供至少40亿CFU罗伊氏乳杆菌NCIMB 30242补充剂,可以降低LDL胆固醇水平,以及hs-CRP、载脂蛋白B-100(apoB-100)(一种与动脉粥样硬化发展相关的脂质成分)和纤维蛋白原水平38,39。同样,在一项包括114名高胆固醇患者的试验中,与安慰剂酸奶相比,一种含有14亿CFU罗伊氏乳杆菌NCIMB 30242的酸奶在六周内每天服用两次,降低了LDL胆固醇、apoB-100和非HDL胆固醇水平40。
其他益生菌菌株已被发现可以改善与血栓形成风险相关的参数。在一项对34名健康人进行的安慰剂对照试验中,连续12周每天饮用含有100亿CFU乳双歧杆菌和600mg精氨酸(一氧化氮的前体)的酸奶,可以改善血管功能,因此被认为可以降低动脉粥样硬化的风险41。一项对36名重度吸烟者进行的安慰剂对照试验发现,连续六周每天饮用200亿CFUs植物乳杆菌的饮料可以降低血压和纤维蛋白原水平,以及炎症细胞因子和氧化应激标志物的水平42。另一项针对32名人类免疫缺陷病毒(HIV)患者的试验比较了每日多菌株益生菌补充剂与安慰剂的效果,8周后,那些服用益生菌的人体内d -二聚体的水平下降幅度更大43。在小鼠中,摄入一种由产生溶栓酶纳豆激酶的枯草芽孢杆菌菌株发酵的奶制品可以减少血栓形成的发生44。
5. 维生素C:
维生素C是一种水溶性抗氧化剂,在实验室的高氧化应激促血栓形成条件下,已证明具有减少血小板聚集和促进纤维蛋白溶解的能力,而不会影响凝血途径45-47。特别是,维生素C似乎会降低内皮细胞和血小板粘附蛋白的表达46,48。一项对20,000多名年龄40-79岁的成年人的大规模研究,对这些人进行了平均9.5年的随访,发现血浆维生素C基线浓度最高的四分之一人群比最低四分之一人中风的风险低42%49。
一项对17项随机对照试验的荟萃分析发现,每天补充500至2000mg维生素C可以改善血管功能50,51。一些证据表明,补充维生素C可能会改善动脉粥样硬化和其他与静脉和动脉血栓风险增加相关的疾病,但这种影响可能是轻微的,对那些维生素C水平较低、心血管风险较高的人来说更为重要50,51。事实上,在连续四周每天两次服用1000mg维生素C后,对慢性心衰患者的血管扩张有积极影响52。
多项研究证明,吸烟者的血液中维生素C水平较低,每天口服2000mg维生素C可显著降低尿中异丙肾上腺素53、一种氧化应激标志物和单核细胞与血管内皮层的粘附,这是危险动脉粥样硬化斑块发展的早期阶段之一54。
6. 碧萝芷:
碧萝芷是一种来自法国海松树皮中的提取物,可预防长途飞行中引起的水肿和静脉血栓形成,并可能有助于慢性静脉不足55,56。在一项对照试验中,198名患有中高静脉血栓形成风险的航空乘客服用了碧萝芷,在长途飞行前和飞行期间服用200mg,第二天服用100mg,或服用安慰剂。安慰剂组有5例静脉血栓形成事件,碧萝芷组没有57。
在一项随机对照试验中,156名有单次DVT发作史的受试者中,150mg碧萝芷在一年后减少水肿方面与压缩袜一样有效,但由于压缩袜的不适,碧萝芷依从性更好58。在一项对222名有深静脉血栓病史的患者随访6年的观察性研究中,每天服用200mg碧萝芷的患者与服用血液稀释剂如阿司匹林、噻氯匹定(Ticlid)、舒洛地特(Aterina)或不服用药物的患者相比,深静脉血栓复发和血栓形成后综合征的风险更低59。碧萝芷还被发现通过增加健康受试者和冠状动脉疾病患者的一氧化氮生成来改善动脉内皮功能60,61。一个研究小组发现,连续两个月每天服用200mg碧萝芷可抑制慢性吸烟者因吸烟引起的血小板聚集升高,但对非吸烟者的血小板聚集没有影响62。
一项对307名有视网膜静脉血栓形成史的受试者进行的观察性研究发现,与阿司匹林、噻氯匹定、舒洛地特或不用药相比,每天服用100mg碧萝芷与复发性视网膜静脉血栓形成的发生率最低相关,并且是唯一与水肿减少相关的治疗方法63。一项类似设计的小型研究发现,与阿司匹林相比,9个月后,每天服用100mg碧萝芷与更好的视力、更低的视网膜水肿和复发性视网膜静脉血栓的风险以及更低的不良副作用发生率相关64。
7. 番茄红素:
番茄红素是一种类胡萝卜素,在番茄皮中含量很高。实验室和动物研究表明,番茄红素可能抑制组织因子活性并抑制血小板聚集65,66。番茄红素被认为可能通过减少内皮损伤、抑制LDL氧化、降低炎症免疫活性等机制预防血栓形成67。一项对28项观察性研究的荟萃分析发现,番茄红素的摄入量或血液水平越高,患中风和心血管疾病的风险越低68。
番茄加工副产品番茄渣含有番茄红素和多种番茄类黄酮,这些活性成分可以共同抑制血小板聚集并降低血栓形成风险69,70。在一项对99名健康年轻男性进行的安慰剂对照试验中,连续五天每天服用1000mg番茄渣提取物,可减少血小板聚集71。
8. 银杏叶:
银杏叶提取物可以刺激外周和冠状动脉循环,并可以预防神经和心血管疾病72-74。研究表明,银杏中的化合物可以减少氧化和炎症性内皮细胞损伤,改善血管功能,抑制动脉粥样硬化斑块的形成,并可能降低动脉血栓的风险75,76。
在一项涉及慢性静脉功能不全导致静脉血栓高风险患者的临床试验中,用银杏提取物治疗导致循环内皮细胞水平降低。循环内皮细胞被认为是血管持续损伤的标志77。证据还表明,银杏可以改善与血栓相关的疾病,包括高血压、不健康的血脂水平和高血糖水平78。
临床前研究表明,银杏提取物可抑制血小板活化因子(参与血小板活化),增加内皮细胞血栓调节蛋白的表达(激活凝血酶)和组织纤溶酶原激活物的产生(刺激纤维蛋白溶解)79,80。另有研究表明,银杏黄酮能直接抑制凝血酶活性81。然而,银杏似乎不会影响出血时间,使用银杏也不会增加出血的风险82,83。
9. 大蒜:
越来越多的研究表明,大蒜可以减缓动脉粥样硬化的进展,改善心脏代谢健康84。大蒜和大蒜提取物可以通过抑制血小板聚集、降低纤维蛋白原水平和增加纤溶过程来降低血栓形成风险85,86。一些证据表明,大蒜中的活性化合物Ajoene (阿霍烯)可能有助于其抗血栓特性87,88。
在一项临床试验中,36名健康的年轻男性每天接受600mg、1200mg或2400mg大蒜提取物或75mg血液稀释剂氯吡格雷,为期三周。接受1200mg或2400mg大蒜的患者的血液样本显示,对各种触发因素的反应,血小板聚集显著减少,并且剂量越高,效果越强。2400 mg剂量的大蒜在抑制血小板对某些但并非所有血栓触发因素的反应方面比氯吡格雷更有效。此外,所有参与者的出血时间都延长了(但保持在正常范围内),其中服用2400 mg大蒜提取物的参与者出血时间最长89。一项为期12周的安慰剂对照试验检查了陈蒜提取物与华法林治疗相结合的安全性。该试验包括48名密切监测的参与者,发现服用陈蒜提取物和华法林不会增加出血或其他不良副作用90。
10.橄榄油和橄榄叶:
特级初榨橄榄油(EVOO)富含单不饱和脂肪酸和抗氧化多酚,高摄入量一直与较低的心血管风险有关91。橄榄油已被证明可以降低氧化应激和炎症标志物水平,改善内皮功能以及脂质和碳水化合物代谢,并抑制血栓形成91,92。临床前研究表明,橄榄油可降低血小板活性和聚集,降低内皮细胞粘附分子的表达,降低凝血酶因子VII和纤溶酶原激活物抑制剂-1,这两者都与冠状动脉疾病有关93。一些证据表明,橄榄油可以减轻通常由高脂肪膳食引起的凝血酶活性的升高94。在一项针对82名早期动脉粥样硬化患者的临床试验中,每天30ml(1盎司)橄榄油,持续四个月,改善了血管功能和炎症标志物水平95。
橄榄多酚(Oleuropein)及其衍生物羟基酪醇(Hydroxytyrosol)是在橄榄、EVOO和橄榄叶中发现的多酚。这些化合物已显示出降低炎症和氧化应激的特性,并被发现可改善血管功能以及葡萄糖和脂质代谢96。多项临床前研究的结果表明,从EVOO和橄榄叶中提取的橄榄蛋白、羟基酪醇和其他酚类物质可抑制血小板活化和聚集97-99。
11.石榴:
石榴富含黄酮类化合物、单宁和其他多酚,具有较强的清除自由基和抗炎特性100。一项对八项随机对照试验的荟萃分析发现,每天饮用230ml石榴汁可以降低收缩压,每天饮用超过230ml石榴汁可以降低收缩和舒张压101。在一项针对13名健康受试者的公开试验中,连续两周每天饮用50ml(约两盎司)石榴汁,可使血小板聚集减少11%102。另一项临床试验发现,饮用石榴汁的受试者6小时后凝血时间延长103。
石榴还被发现可以减少氧化应激和高血压,并改善血管功能和糖脂代谢104,105。一项针对100名心脏病患者的随机安慰剂对照试验发现,每天450mg石榴提取物加180mg维生素E(dl-α-生育酚),持续8周,可降低两种血管粘附蛋白的表达,降低炎症标记物的水平106。另一项试验包括48名超重或肥胖的受试者,服用1000mg石榴提取物30天,可降低炎症标志物水平,改善血糖、胰岛素和LDL胆固醇水平107。
12.可可:
可可富含黄烷醇和其他多酚类物质,具有很强的自由基清除作用。研究发现,可可和黑巧克力可以降低血小板活化,抑制参与血小板聚集的蛋白质表达,并限制血小板活性对止血的影响108,109。可可除了含有多酚外,还含有可可碱(或咖啡碱),可可碱是甲基黄嘌呤家族中的一种化合物,也能抑制血小板聚集109。临床试验发现,可可中的多酚可以增加一氧化氮的产生,支持健康的内皮功能,降低炎症标志物水平,减少对脂质的氧化损伤,促进肠道有益细菌的生长110,111。
在健康男性的临床试验中,吃50g含有90%可可的巧克力,可以降低血小板反应性,延长四小时后采集的血液样本的凝血时间112,113。另一项临床试验发现,在健康男性中,食用黑巧克力可以抑制由实验性心理压力引起的d -二聚体水平的上升114。在一项针对健康中年人的开放标签对照试验中,每天900mg可可黄烷醇,持续30天,可改善内皮功能,这是血栓形成风险的一个重要因素;在后续的一项对照试验中,相同剂量也显示可改善血压和血脂水平115。
一项随机对照试验发现,在冠心病患者服用30天后,每天提供750mg黄烷醇的可可比低黄烷醇可可更能改善血管功能和内皮完整性标志物116。此外,富含黄烷醇的可可还被发现可以改善年轻的非裔美国人117、健康年轻群体118、绝经后妇女119、终末期肾病患者120、高血压男性121、健康的老年男性的血管功能122。
13. 绿茶:
绿茶被研究最多的是绿茶多酚(EGCG,表没食子儿茶素没食子酸酯)。临床试验和观察性研究发现,绿茶与降低心血管风险有关,因为它增加了一氧化氮的可用性,减少了炎症和氧化应激水平,改善了内皮功能123,124。
采用服用过血液稀释剂阿司匹林、氯吡格雷或替格瑞洛(Brilinta)的受试者血液样本进行的研究表明,EGCG可以在不增加出血风险的情况下改善其抗血小板作用125。EGCG已被证明可以抑制血小板中的炎症酶活性126,抑制炎症信号以及粘附分子的表达,促进内皮细胞中核因子红细胞2相关因子2 (Nrf2,一种上调抗氧化途径的蛋白)的表达123,127。EGCG还能抑制组织因子(一种触发动脉和静脉内皮细胞凝血的蛋白质)的表达128。
14. 槲皮素:
槲皮素是一种黄酮类化合物,存在于大多数水果和蔬菜中,在洋葱、苹果和葡萄酒中含量很高。黄酮类化合物(包括槲皮素)的摄入量越高,心血管风险越低129。研究发现,在健康成人中,补充150mg和300mg剂量的槲皮素可在30分钟内抑制血小板活化、信号传导和聚集130。在六周内补充150mg槲皮素也被证明可以显著降低收缩压和氧化LDL水平131。
临床前研究表明,槲皮素可以降低内皮细胞和血小板上粘附分子的表达,降低氧化应激,抑制LDL氧化,支持一氧化氮生成和健康血管功能,改善葡萄糖代谢,降低炎症标志物水平129,132。槲皮素和其他类黄酮被认为是蜂产品蜂胶和特种蜂蜜的抗血栓和心脏保护特性的原因133,134。
15. 生姜:
生姜是一种烹饪香料和草药,在临床上已证明具有心脏保护作用,如提高脂质水平、降低炎症细胞因子水平、降低血压和抑制血小板聚集135,136。一项观察性研究检查了4628名参与者的健康记录和饮食调查,发现在60岁及以上的人群中,那些报告较多使用生姜的人患冠状动脉疾病的几率较低137。生姜也可能对肥胖和2型糖尿病等代谢紊乱有益138。在一项对小鼠的研究中,姜酮(生姜的一种活性化合物)不仅抑制血小板聚集,还抑制因子Xa的活性,凝血过程中的一种酶139。实验室研究还发现,从生姜中提取的一种多糖抑制了凝血途径140。由于样本量小,使用的方法多变,对八项临床试验的系统综述无法就生姜对人类血小板聚集的影响得出确切结论141。在其中一项试验中,服用4g生姜三个月不会改变冠状动脉疾病患者的血小板聚集、纤维蛋白原水平或纤溶活性,但单次服用10g生姜会减少血小板聚集142。
16. 卡宴椒:
其所含辣椒素是一种活性化合物。辣椒素用于治疗炎症、代谢和感染性疾病143。临床前和临床证据表明,辣椒素可以改善脂质和葡萄糖代谢,支持减肥,并降低患2型糖尿病和心血管疾病的风险143-145。实验室证据表明,辣椒素有可能减少血小板聚集,而不影响凝血145,146。然而,在健康男性志愿者中,400 mcg和800 mcg的辣椒素都不影响血小板聚集147。
17. 姜黄素:
姜黄素是一种在烹饪香料姜黄中发现的类胡萝卜素,具有减少氧化应激和抗炎的特性。其潜在的抗血栓作用(包括抗血小板和抗凝)已在实验室和动物研究中得到证实148,149。一项临床前研究的结果表明,姜黄素可能有助于促进内皮修复和静脉血栓的解决150。在小鼠中,用姜黄素治疗可以防止炎症因子的增加,血压和暴露在空气污染(柴油废气)中的D-二聚体,这是一种已知会增加炎症和血栓风险的常见环境因素151。
18. 亚洲参:
在中国,三七提取物被静脉注射用于治疗急性血栓形成,一些证据表明,人参的口服提取物也可能具有抗血栓作用。生物活性皂苷,即人参皂苷,存在于中国人参、红参和西洋参中152-154。在一项为期28天的临床试验中发现了一种人参皂苷的口服制剂,可以减少血小板聚集155。
临床前研究表明,人参皂苷可以抑制血小板粘附分子的表达,血小板聚集和血小板对血栓触发物的反应性,这可能提供对过度血液凝结的保护156,157。此外,在实验室和动物研究中,人参皂苷已被证明可以减少血管炎症和僵硬,稳定动脉粥样硬化斑块,减缓动脉粥样硬化进展,这可能有助于预防血栓栓塞158。人参皂甙还可以通过减少自由基的产生、增加一氧化氮、增加血管内皮细胞的功能来改善血管功能,和调节脂质水平152。人参和人参皂苷具有抗炎和广泛的健康促进作用,可能有益于与血栓形成风险相关的个体152,159。人参中的其他化合物可能进一步促进其抗血小板活性160。
19. 马黛茶:
马黛茶富含抗炎和清除自由基特性的绿原酸161。在一项针对142名血液粘度高参与者的随机安慰剂对照试验中,6周内每天5g马黛茶可降低血液粘度,改善小血管的循环162。另一项对照临床试验发现,每天580mg马黛茶中的绿原酸可改善34名代谢综合征高危中年男性的心脏代谢健康标志物163。在临床前研究中,马黛茶的一种成分降低了凝血酶活化和静脉血栓形成164。
更多可点击其个性化的综合干预方案如下:
- 血栓管理要略(抗血凝)
- 血栓管理要略(抑制血小板)
- 血栓管理要略(控制纤维蛋白原)
- 血栓管理要略(溶解血凝块)
- 防止血栓形成(50-60岁)
- 防止血栓形成(61-70岁)
- 防止血栓形成(71-80岁)
- 防止血栓形成(81岁以上)
以及参阅本网如下专文的相关内容:
医疗干预
两类药物可降低血栓形成及其并发症风险,作为第三类的血栓溶解剂/纤维蛋白溶解剂(阿替普酶,tPA)一般用于医疗急救如脑梗塞、肺栓塞和心脏病发作等,可破坏血栓并减少组织损伤。
- 抗血小板药:抑制血小板活化和聚集。
- 阿司匹林,最常用抗血小板药,可阻止血小板聚集。低剂量阿司匹林可有效降低病理性血栓形成的风险,同时保持最佳的内皮功能。
- 氯吡格雷:抑制血小板被激活,且在减少血小板聚集方面比阿司匹林更有效。如果不能忍受阿司匹林副作用时,医生一般推荐此药物。
- 抗凝血药:抑制纤维蛋白原转化为纤维蛋白,这是凝血过程中稳定血栓的最后步骤之一。
- 华法林:一种强效的抗凝血剂,与多种药物甚至食物、营养剂等存在相互作用的风险。
- 肝素:一种天然抗凝血剂,可刺激抗凝血酶活性,并防止纤维蛋白原分子聚集成纤维蛋白。肝素及其衍生物通过注射给药。
- 其他新型抗凝血药,包括如:达比加群(Dabigatran),利伐沙班( Rivaroxaban )和阿哌沙班(Apixaban)等。
参考文献:
1. Golanski J et al. Effects of Omega-3 Polyunsaturated Fatty Acids and Their Metabolites on Haemostasis-Current Perspectives in Cardiovascular Disease. International journal of molecular sciences. Feb 27 2021;22(5)
2. Fan H et al. Meta-Analysis Comparing the Effect of Combined Omega-3 + Statin Therapy Versus Statin Therapy Alone on Coronary Artery Plaques. Am J Cardiol. 2021 Jul 15;151:15-24.
3. Bernasconi AA et al. Effect of Omega-3 Dosage on Cardiovascular Outcomes: An Updated Meta-Analysis and Meta-Regression of Interventional Trials. Mayo Clin Proc. Feb 2021;96(2):304-313.
4. Saber H et al. Omega-3 Fatty Acids and Incident Ischemic Stroke and Its Atherothrombotic and Cardioembolic Subtypes in 3 US Cohorts. Stroke. Oct 2017;48(10):2678-2685.
5. Lombardi M et al. Impact of Different Doses of Omega-3 Fatty Acids on Cardiovascular Outcomes: a Pairwise and Network Meta-analysis. Curr Atheroscler Rep. Jul 16 2020;22(9):45.
6. Zheng X et. Omega-3 fatty acids reduce post-operative risk of deep vein thrombosis and pulmonary embolism after surgery for elderly patients with proximal femoral fractures: a randomized placebo-controlled, double-blind clinical trial. Int Orthop. Oct 2020;44(10):2089-2093.
7. Viecelli AK et al. Fish oil and aspirin effects on arteriovenous fistula function: Secondary outcomes of the randomised omega-3 fatty acids (Fish oils) and Aspirin in Vascular access OUtcomes in REnal Disease (FAVOURED) trial. PLoS One. 2019;14(3):e0213274.
8. Isaksen T et al. Dietary intake of marine n-3 polyunsaturated fatty acids and future risk of venous thromboembolism. Research and practice in thrombosis and haemostasis. Jan 2019;3(1):59-69.
9. Isaksen T, Evensen LH, Brækkan SK, Hansen JB. Dietary Intake of Marine Polyunsaturated n-3 Fatty Acids and Risk of Recurrent Venous Thromboembolism. Thrombosis and haemostasis. Dec 2019;119(12):2053-2063.
10. Reiner MF et al. Omega-3 fatty acids predict recurrent venous thromboembolism or total mortality in elderly patients with acute venous thromboembolism. J Thromb Haemost. Jan 2017;15(1):47-56.
11. Shimizu M et al. Low coenzyme Q10 levels in patients with acute cardiovascular disease are associated with long-term mortality. Heart Vessels. Mar 2021;36(3):401-407.
12. Martelli A et al. Coenzyme Q(10): Clinical Applications in Cardiovascular Diseases. Antioxidants (Basel, Switzerland). Apr 22 2020;9(4)
13. Rabanal-Ruiz Y et al. The Use of Coenzyme Q10 in Cardiovascular Diseases. Antioxidants (Basel, Switzerland). May 10 2021;10(5)
14. Arenas-Jal M et al. Coenzyme Q10 supplementation: Efficacy, safety, and formulation challenges. Compr Rev Food Sci Food Saf. Mar 2020;19(2):574-594.
15. Ya F et al. Coenzyme Q10 Upregulates Platelet cAMP/PKA Pathway and Attenuates Integrin αIIbβ3 Signaling and Thrombus Growth. Mol Nutr Food Res. Dec 2019;63(23):e1900662.
16. Raizner AE et al. Coenzyme Q(10) for Patients With Cardiovascular Disease: JACC Focus Seminar. Journal of the American College of Cardiology. Feb 9 2021;77(5):609-619.
17. Alehagen U et al. Dietary Supplementation with Selenium and Coenzyme Q(10) Prevents Increase in Plasma D-Dimer While Lowering Cardiovascular Mortality in an Elderly Swedish Population. Nutrients. Apr 17 2021;13(4)
18. Alehagen U et al. Significant decrease of von Willebrand factor and plasminogen activator inhibitor-1 by providing supplementation with selenium and coenzyme Q10 to an elderly population with a low selenium status. European journal of nutrition. 2020/12/01 2020;59(8):3581-3590.
19. Sabbatinelli J et al. Ubiquinol Ameliorates Endothelial Dysfunction in Subjects with Mild-to-Moderate Dyslipidemia: A Randomized Clinical Trial. Nutrients. Apr 15 2020;12(4)
20. Pérez-Sánchez C et al. Ubiquinol Effects on Antiphospholipid Syndrome Prothrombotic Profile: A Randomized, Placebo-Controlled Trial. Arteriosclerosis, thrombosis, and vascular biology. Oct 2017;37(10):1923-1932.
21. Ramirez A et al. Low High-Density Lipoprotein and Risk of Myocardial Infarction. Clinical Medicine Insights Cardiology. 2015;9:113-7.
22. Subedi BH et al. Current guidelines for high-density lipoprotein cholesterol in therapy and future directions. Vasc Health Risk Manag. 2014;10:205-16. doi:10.2147/vhrm.S45648
23. Probstfield JL, Boden WE, Anderson T, et al. Cardiovascular outcomes during extended follow-up of the AIM-HIGH trial cohort. Journal of clinical lipidology. Nov-Dec 2018;12(6):1413-1419.
24. Landray MJ, Haynes R, Hopewell JC, et al. Effects of extended-release niacin with laropiprant in high-risk patients. The New England journal of medicine. Jul 17 2014;371(3):203-12.
25. Zeman M et al. Pleiotropic effects of niacin: Current possibilities for its clinical use. Acta pharmaceutica (Zagreb, Croatia). Dec 1 2016;66(4):449-469.
26. Zhou K et al. Association between B-group vitamins and venous thrombosis: systematic review and meta-analysis of epidemiological studies. Journal of thrombosis and thrombolysis. Nov 2012;34(4):459-67.
27. Zaric BL et al. Homocysteine and Hyperhomocysteinaemia. Curr Med Chem. 2019;26(16):2948-2961.
28. Amaral FM et al. Interactions among methylenetetrahydrofolate reductase (MTHFR) and cystathionine β-synthase (CBS) polymorphisms - a cross-sectional study: multiple heterozygosis as a risk factor for higher homocysteine levels and vaso-occlusive episodes. Genetics and molecular research Feb 23 2017;16(1)
29. Spence JD. Cardioembolic stroke: everything has changed. Stroke Vasc Neurol. Jun 2018;3(2):76-83.
30. Ammouri W et al. Venous thromboembolism and hyperhomocysteinemia as first manifestation of pernicious anemia: a case series. Journal of medical case reports. Sep 2 2017;11(1):250.
31. Prajapati K et al. Pernicious anaemia: cause of recurrent cerebral venous thrombosis. BMJ case reports. May 10 2021;14(5)
32. Spence JD. Homocysteine lowering for stroke prevention: Unravelling the complexity of the evidence. Int J Stroke. Oct 2016;11(7):744-7
33. Kong X et al. Platelet Count Affects Efficacy of Folic Acid in Preventing First Stroke. Journal of the American College of Cardiology. May 15 2018;71(19):2136-2146.
34. Shu XJ et al. Effects of folic acid combined with vitamin B12 on DVT in patients with homocysteine cerebral infarction. European review for medical and pharmacological sciences. May 2017;21(10):2538-2544.
35. Lässiger-Herfurth A et al. The Gut Microbiota in Cardiovascular Disease and Arterial Thrombosis. Microorganisms. Dec 13 2019;7(12)
36. Lippi G et al. The Intriguing Link between the Intestinal Microbiota and Cardiovascular Disease. Semin Thromb Hemost. Sep 2017;43(6):609-613.
37. Wu Y et al. Effect of probiotic Lactobacillus on lipid profile: A systematic review and meta-analysis of randomized, controlled trials. PLoS One. 2017;12(6):e0178868.
38. Jones ML et al. Cholesterol lowering and inhibition of sterol absorption by Lactobacillus reuteri NCIMB 30242: a randomized controlled trial. Eur J Clin Nutr. Nov 2012;66(11):1234-41.
39. Jones ML et al. Oral supplementation with probiotic L. reuteri NCIMB 30242 increases mean circulating 25-hydroxyvitamin D: a post hoc analysis of a randomized controlled trial. J Clin Endocrinol Metab. Jul 2013;98(7):2944-51. doi:10.1210/jc.2012-4262
40. Jones ML et al. Cholesterol-lowering efficacy of a microencapsulated bile salt hydrolase-active Lactobacillus reuteri NCIMB 30242 yoghurt formulation in hypercholesterolaemic adults. Br J Nutr. May 2012;107(10):1505-13.
41. Matsumoto M et al. Endothelial Function is improved by Inducing Microbial Polyamine Production in the Gut: A Randomized Placebo-Controlled Trial. Nutrients. May 27 2019;11(5)
42. Naruszewicz M et al. Effect of Lactobacillus plantarum 299v on cardiovascular disease risk factors in smokers. Am J Clin Nutr. Dec 2002;76(6):1249-55.
43. Stiksrud B et al. Reduced Levels of D-dimer and Changes in Gut Microbiota Composition After Probiotic Intervention in HIV-Infected Individuals on Stable ART. J Acquir Immune Defic Syndr. Dec 1 2015;70(4):329-37.
44. Zhang X et al. Screening of a Bacillus subtilis strain producing both nattokinase and milk-clotting enzyme and its application in fermented milk with thrombolytic activity. J Dairy Sci. Jul 1 2021;doi:10.3168/jds.2020-19756
45. Liu D et al. Effects and Mechanisms of Vitamin C Post-Conditioning on Platelet Activation after Hypoxia/Reoxygenation. Transfus Med Hemother. Apr 2020;47(2):110-118.
46. Tyml K. Vitamin C and Microvascular Dysfunction in Systemic Inflammation. Antioxidants (Basel, Switzerland). Jun 29 2017;6(3)
47. Mohammed BM et al. Impact of high dose vitamin C on platelet function. World journal of critical care medicine. Feb 4 2017;6(1):37-47.
48. Secor D et al. Ascorbate inhibits platelet-endothelial adhesion in an in-vitro model of sepsis via reduced endothelial surface P-selectin expression. Blood Coagul Fibrinolysis. Jan 2017;28(1):28-33.
49. Ashor AW et al. Effect of vitamin C and vitamin E supplementation on endothelial function: a systematic review and meta-analysis of randomized controlled trials. The British journal of nutrition. Apr 28 2015;113(8):1182-94.
50. Ashor AW et al. Limited evidence for a beneficial effect of vitamin C supplementation on biomarkers of cardiovascular diseases: an umbrella review of systematic reviews and meta-analyses. Nutr Res. Jan 2019;61:1-
51. Moser MA et al. Vitamin C and Heart Health: A Review Based on Findings from Epidemiologic Studies. International journal of molecular sciences. Aug 12 2016;17(8)
52. Hornig B et al. Vitamin C improves endothelial function of conduit arteries in patients with chronic heart failure. Circulation. Feb 3 1998;97(4):363-8.
53. Reilly M et al. Modulation of oxidant stress in vivo in chronic cigarette smokers. Circulation. Jul 1 1996;94(1):19-25.
54. Weber C et al. Increased adhesiveness of isolated monocytes to endothelium is prevented by vitamin C intake in smokers. Circulation. Apr 15 1996;93(8):1488-92.
55. Gulati OP. Pycnogenol® in chronic venous insufficiency and related venous disorders. Phytother Res. Mar 2014;28(3):348-62.
56. Belcaro G et al. Long-haul flights, edema, and thrombotic events: prevention with stockings and Pycnogenol® supplementation (LONFLIT Registry Study). Minerva cardioangiologica. Apr 2018;66(2):152-159.
57. Belcaro G et al. Prevention of venous thrombosis and thrombophlebitis in long-haul flights with pycnogenol. Clinical and applied thrombosis/hemostasis. Oct 2004;10(4):373-7.
58. Errichi BM et al. Prevention of post thrombotic syndrome with Pycnogenol® in a twelve month study. Panminerva medica. Sep 2011;53(3 Suppl 1):21-7.
59. Belcaro G et al. Prevention of recurrent venous thrombosis and post-thrombotic syndrome. Minerva cardioangiologica. Jun 2018;66(3):238-245.
60. Nishioka K et al. Pycnogenol, French maritime pine bark extract, augments endothelium-dependent vasodilation in humans. Hypertension research Sep 2007;30(9):775-80.
61. Enseleit F et al. Effects of Pycnogenol on endothelial function in patients with stable coronary artery disease: a double-blind, randomized, placebo-controlled, cross-over study. Eur Heart J. Jul 2012;33(13):1589-97.
62. Araghi-Niknam M et al. Pine bark extract reduces platelet aggregation. Integrative medicine . Mar 21 2000;2(2):73-77.
63. Belcaro G et al. Recurrent retinal vein thrombosis: prevention with Aspirin, Pycnogenol®, ticlopidine, or sulodexide. Minerva cardioangiologica. Apr 2019;67(2):109-114. doi:10.23736/s0026-4725.19.04891-6
64. Rodriguez P et al. Recurrence of retinal vein thrombosis with Pycnogenol® or Aspirin® supplementation: a registry study. Panminerva medica. Sep 2015;57(3):121-5.
65. Lee DK et al. Carotenoids enhance phosphorylation of Akt and suppress tissue factor activity in human endothelial cells. J Nutr Biochem. Nov 2006;17(11):780-6.
66. Sawardekar SB et al. Comparative evaluation of antiplatelet effect of lycopene with aspirin and the effect of their combination on platelet aggregation: An in vitro study. Indian journal of pharmacology. Jan-Feb 2016;48(1):26-31.
67. Thies F et al. Cardiovascular benefits of lycopene: fantasy or reality? The Proceedings of the Nutrition Society. May 2017;76(2):122-129.
68. Cheng HM et al. Lycopene and tomato and risk of cardiovascular diseases: A systematic review and meta-analysis of epidemiological evidence. Crit Rev Food Sci Nutr. 2019;59(1):141-158.
69. Concha-Meyer A et al. Platelet Anti-Aggregant Activity and Bioactive Compounds of Ultrasound-Assisted Extracts from Whole and Seedless Tomato Pomace. Foods. Oct 28 2020;9(11)
70. Fuentes E et al. Antiplatelet effects of bioactive compounds present in tomato pomace. Current drug targets. Jan 28 2021;
71. Palomo I et al. Chemical Characterization and Antiplatelet Potential of Bioactive Extract from Tomato Pomace (Byproduct of Tomato Paste). Nutrients. Feb 22 2019;11(2)
72. Zuo W et al. Advances in the Studies of Ginkgo Biloba Leaves Extract on Aging-Related Diseases. Aging Dis. Dec 2017;8(6):812-826.
73. Wu Y et al. Ginkgo biloba extract improves coronary blood flow in healthy elderly adults: role of endothelium-dependent vasodilation. Phytomedicine. Mar 2008;15(3):164-9.
74. Jung F et al. Effect of Ginkgo biloba on fluidity of blood and peripheral microcirculation in volunteers. Arzneimittel-Forschung. May 1990;40(5):589-93.
75. Sarkar C et al. Therapeutic promises of ginkgolide A: A literature-based review. Biomedicine & pharmacotherapy. Dec 2020;132:110908
76. Li X et al. New Insight into the Mechanisms of Ginkgo Biloba Extract in Vascular Aging Prevention. Curr Vasc Pharmacol. 2020;18(4):334-345.
77. Janssens D et al. Increase in circulating endothelial cells in patients with primary chronic venous insufficiency: protective effect of Ginkor Fort in a randomized double-blind, placebo-controlled clinical trial. Journal of cardiovascular pharmacology. Jan 1999;33(1):7-11.
78. Eisvand F et al. The effects of Ginkgo biloba on metabolic syndrome: A review. Phytother Res. Aug 2020;34(8):1798-1811.
79. Tian J et al. Ginkgo biloba Extract in Vascular Protection: Molecular Mechanisms and Clinical Applications. Curr Vasc Pharmacol. 2017;15(6):532-548.
80. Chiu YL et al. Ginkgo biloba Induces Thrombomodulin Expression and Tissue-Type Plasminogen Activator Secretion via the Activation of Krüppel-Like Factor 2 within Endothelial Cells. The American journal of Chinese medicine. 2020;48(2):357-372.
81. Chen TR et al. Biflavones from Ginkgo biloba as inhibitors of human thrombin. Bioorganic chemistry. Nov 2019;92:103199.
82. Kellermann AJ et al. Is there a risk of bleeding associated with standardized Ginkgo biloba extract therapy? A systematic review and meta-analysis. Pharmacotherapy. May 2011;31(5):490-502.
83. Ryu KH et al. Ginkgo biloba extract enhances antiplatelet and antithrombotic effects of cilostazol without prolongation of bleeding time. Thromb Res. Jul 2009;124(3):328-34.
84. Ansary J et al. Potential Health Benefit of Garlic Based on Human Intervention Studies: A Brief Overview. Antioxidants (Basel, Switzerland). Jul 15 2020;9(7)
85. Sobenin IA et al. Therapeutic effects of garlic in cardiovascular atherosclerotic disease. Chinese journal of natural medicines. Oct 2019;17(10):721-728.
86. Olas B. Anti-Aggregatory Potential of Selected Vegetables-Promising Dietary Components for the Prevention and Treatment of Cardiovascular Disease. Adv Nutr. Mar 1 2019;10(2):280-290.
87. Apitz-Castro R et al. A garlic derivative, ajoene, inhibits platelet deposition on severely damaged vessel wall in an in vivo porcine experimental model. Thromb Res. Aug 1 1994;75(3):243-9.
88. Apitz-Castro R et al. Effect of ajoene, the major antiplatelet compound from garlic, on platelet thrombus formation. Thromb Res. Oct 15 1992;68(2):145-55.
89. Fakhar H et al. Effect of the Garlic Pill in comparison with Plavix on Platelet Aggregation and Bleeding Time. Iran J Ped Hematol Oncol. 2012;2(4):146-52.
90. Macan H et al. Aged garlic extract may be safe for patients on warfarin therapy. J Nutr. Mar 2006;136(3 Suppl):793s-795s.
91. Katsiki N et al. Olive Oil Intake and Cardiovascular Disease Prevention: "Seek and You Shall Find". Current cardiology reports. May 7 2021;23(6):64.
92. Summerhill V et al. Vasculoprotective Role of Olive Oil Compounds via Modulation of Oxidative Stress in Atherosclerosis. Front Cardiovasc Med. 2018;5:188.
93. Cicerale S et al. Biological activities of phenolic compounds present in virgin olive oil. International journal of molecular sciences. Feb 2 2010;11(2):458-79.
94. Capurso C et al. Vascular effects of the Mediterranean diet part I: anti-hypertensive and anti-thrombotic effects. Vascul Pharmacol. Dec 2014;63(3):118-26.
95. Widmer RJ et al. Beneficial effects of polyphenol-rich olive oil in patients with early atherosclerosis. European journal of nutrition. Apr 2013;52(3):1223-31.
96. Peyrol J et al. Hydroxytyrosol in the Prevention of the Metabolic Syndrome and Related Disorders. Nutrients. Mar 20 2017;9(3)
97. Mizutani D et al. Olive polyphenol reduces the collagen-elicited release of phosphorylated HSP27 from human platelets. Bioscience, biotechnology, and biochemistry. Mar 2020;84(3):536-543.
98. Dell'Agli M et al. Inhibition of platelet aggregation by olive oil phenols via cAMP-phosphodiesterase. The British journal of nutrition. May 2008;99(5):945-51.
99. Singh I et al. The effects of polyphenols in olive leaves on platelet function. Nutr Metab Cardiovasc Dis. Feb 2008;18(2):127-32.
100. Fourati M et al. Bioactive Compounds and Pharmacological Potential of Pomegranate (Punica granatum) Seeds - A Review. Plant foods for human nutrition (Dordrecht, Netherlands). Dec 2020;75(4):477-486.
101. Sahebkar A et al. Effects of pomegranate juice on blood pressure: A systematic review and meta-analysis of randomized controlled trials. Pharmacological research : the official journal of the Italian Pharmacological Society . Jan 2017;115:149-161.
102. Aviram M et al. Pomegranate juice consumption reduces oxidative stress, atherogenic modifications to LDL, and platelet aggregation: studies in humans and in atherosclerotic apolipoprotein E-deficient mice. Am J Clin Nutr. May 2000;71(5):1062-76.
103. Polagruto JA et al. Effects of flavonoid-rich beverages on prostacyclin synthesis in humans and human aortic endothelial cells: association with ex vivo platelet function. Journal of medicinal food. Winter 2003;6(4):301-8.
104. Wang D et al. Vasculoprotective Effects of Pomegranate (Punica granatum L.). Front Pharmacol. 2018;9:544.
105. Delgado NTB et al. Protective Effects of Pomegranate in Endothelial Dysfunction. Curr Pharm Des. 2020;26(30):3684-3699.
106. Jafari T et al. Effects of pomegranate peel extract and vitamin E on the inflammatory status and endothelial function in hemodialysis patients: a randomized controlled clinical trial. Food Funct. Sep 23 2020;11(9):7987-7993.
107. Hosseini B et al. Effects of pomegranate extract supplementation on inflammation in overweight and obese individuals: A randomized controlled clinical trial. Complementary therapies in clinical practice. Feb 2016;22:44-50.
108. Magrone T et al. Cocoa and Dark Chocolate Polyphenols: From Biology to Clinical Applications. Front Immunol. 2017;8:677.
109. Aprotosoaie AC et al. The Cardiovascular Effects of Cocoa Polyphenols-An Overview. Diseases. Dec 17 2016;4(4)
110. Davinelli S et al. Short-term supplementation with flavanol-rich cocoa improves lipid profile, antioxidant status and positively influences the AA/EPA ratio in healthy subjects. J Nutr Biochem. Nov 2018;61:33-39.
111. Tzounis X et al. Prebiotic evaluation of cocoa-derived flavanols in healthy humans by using a randomized, controlled, double-blind, crossover intervention study. Am J Clin Nutr. Jan 2011;93(1):62-72.
112. Montagnana M et al. Dark chocolate modulates platelet function with a mechanism mediated by flavan-3-ol metabolites. Medicine. Dec 2018;97(49):e13432.
113. Montagnana M et al. Short-term effect of dark chocolate consumption on routine haemostasis testing. International journal of food sciences and nutrition. Aug 2017;68(5):613-616.
114. Von Känel R et al. Effects of dark chocolate consumption on the prothrombotic response to acute psychosocial stress in healthy men. Thrombosis and haemostasis. Dec 2014;112(6):1151-8.
115. Sansone R et al. Cocoa flavanol intake improves endothelial function and Framingham Risk Score in healthy men and women: a randomised, controlled, double-masked trial: the Flaviola Health Study. The British journal of nutrition. Oct 28 2015;114(8):1246-55.
116. Horn P et al. Dietary flavanol intervention lowers the levels of endothelial microparticles in coronary artery disease patients. The British journal of nutrition. Apr 14 2014;111(7):1245-52.
117. Kim K et al. Acute consumption of flavanol-rich cocoa beverage improves attenuated cutaneous microvascular function in healthy young African Americans. Microvascular research. Mar 2020;128:103931.
118. Pereira T et al. Randomized study of the effects of cocoa-rich chocolate on the ventricle-arterial coupling and vascular function of young, healthy adults. Nutrition (Burbank, Los Angeles County, Calif). Jul-Aug 2019;63-64:175-183.
119. Okamoto T, Kobayashi R, Natsume M, Nakazato K. Habitual cocoa intake reduces arterial stiffness in postmenopausal women regardless of intake frequency: a randomized parallel-group study. Clin Interv Aging. 2016;11:1645-1652.
120. Rassaf T et al. Vasculoprotective Effects of Dietary Cocoa Flavanols in Patients on Hemodialysis: A Double-Blind, Randomized, Placebo-Controlled Trial. Clinical journal of the American Society of Nephrology : CJASN. Jan 7 2016;11(1):108-18.
121. Rull G et al. Effects of high flavanol dark chocolate on cardiovascular function and platelet aggregation. Vascul Pharmacol. Aug 2015;71:70-8.
122. Heiss C et al. Impact of cocoa flavanol intake on age-dependent vascular stiffness in healthy men: a randomized, controlled, double-masked trial. Age (Dordr). Jun 2015;37(3):9794.
123. Yamagata K. Protective Effect of Epigallocatechin Gallate on Endothelial Disorders in Atherosclerosis. Journal of cardiovascular pharmacology. Apr 2020;75(4):292-298.
124. Slevin M et al. Unique vascular protective properties of natural products: supplements or future main-line drugs with significant anti-atherosclerotic potential? Vasc Cell. Apr 30 2012;4(1):9.
125. Joo HJ et al. Anti-platelet effects of epigallocatechin-3-gallate in addition to the concomitant aspirin, clopidogrel or ticagrelor treatment. The Korean journal of internal medicine. May 2018;33(3):522-531.
126. Lee DH et al. Inhibitory effects of epigallocatechin-3-gallate on microsomal cyclooxygenase-1 activity in platelets. Biomolecules & therapeutics. Jan 2013;21(1):54-9.
127. Reddy AT et al. Epigallocatechin gallate suppresses inflammation in human coronary artery endothelial cells by inhibiting NF-κB. Life Sci. Oct 1 2020;258:118136.
128. Zhang Z et al. Potential protective mechanisms of green tea polyphenol EGCG against COVID-19. Trends Food Sci Technol. Aug 2021;114:11-24.
129. Anand David AV et al. Overviews of Biological Importance of Quercetin: A Bioactive Flavonoid. Pharmacogn Rev. Jul-Dec 2016;10(20):84-89.
130. Hubbard GP et al. Ingestion of quercetin inhibits platelet aggregation and essential components of the collagen-stimulated platelet activation pathway in humans. J Thromb Haemost. Dec 2004;2(12):2138-45.
131. Egert S et al. Quercetin reduces systolic blood pressure and plasma oxidized low-density lipoprotein concentrations in overweight subjects with a high-cardiovascular disease risk phenotype: a double-blinded, placebo-controlled cross-over study. The British journal of nutrition. Oct 2009;102(7):1065-74.
132. Patel RV et al. Therapeutic potential of quercetin as a cardiovascular agent. European journal of medicinal chemistry. Jul 15 2018;155:889-904.
133. Zhang YX et al. Inhibitory Effect of Propolis on Platelet Aggregation In Vitro. J Healthc Eng. 2017;2017:3050895.
134. Olas B. Honey and Its Phenolic Compounds as an Effective Natural Medicine for Cardiovascular Diseases in Humans? Nutrients. Jan 21 2020;12(2)doi:10.3390/nu12020283
135. Li C et al. Vasculoprotective effects of ginger (Zingiber officinale Roscoe) and underlying molecular mechanisms. Food Funct . Mar 15 2021;12(5):1897-1913.
136. Fakhri S et al. Ginger and Heart Health: From Mechanisms to Therapeutics. Current molecular pharmacology. 2021;14(6):943-959.
137. Wang Y et al. Evaluation of daily ginger consumption for the prevention of chronic diseases in adults: A cross-sectional study. Nutrition (Burbank, Los Angeles County, Calif). Apr 2017;36:79-84.
138. Mao QQ et al. Bioactive Compounds and Bioactivities of Ginger (Zingiber officinale Roscoe). Foods. May 30 2019;8(6)
139. Lee W et al. Anti-factor Xa activities of zingerone with anti-platelet aggregation activity. Food and chemical toxicology Jul 2017;105:186-193.
140. Wang C et al. Sulfation, structural analysis, and anticoagulant bioactivity of ginger polysaccharides. Journal of food science. Aug 2020;85(8):2427-2434.
141. Marx W et al. The Effect of Ginger (Zingiber officinale) on Platelet Aggregation: A Systematic Literature Review. PLoS One. 2015;10(10):e0141119.
142. Bordia A et al. Effect of ginger (Zingiber officinale Rosc.) and fenugreek (Trigonella foenumgraecum L.) on blood lipids, blood sugar and platelet aggregation in patients with coronary artery disease. Prostaglandins Leukot Essent Fatty Acids. May 1997;56(5):379-84.
143. Sanati S et al. A review of the effects of Capsicum annuum L. and its constituent, capsaicin, in metabolic syndrome. Iranian journal of basic medical sciences. May 2018;21(5):439-448.
144. Panchal SK et al. Capsaicin in Metabolic Syndrome. Nutrients. May 17 2018;10(5)
145. Fattori V et al. Capsaicin: Current Understanding of Its Mechanisms and Therapy of Pain and Other Pre-Clinical and Clinical Uses. Molecules (Basel, Switzerland). Jun 28 2016;21(7)
146. Almaghrabi S et al. Synergistic inhibitory effect of capsaicin and dihydrocapsaicin on in-vitro platelet aggregation and thromboxane formation. Blood Coagul Fibrinolysis. Jun 2018;29(4):351-355.
147. Sandor B et al. Orally given gastroprotective capsaicin does not modify aspirin-induced platelet aggregation in healthy male volunteers (human phase I examination). Acta physiologica Hungarica. Dec 2014;101(4):429-37.
148. Keihanian F et al. Curcumin, hemostasis, thrombosis, and coagulation. J Cell Physiol. Jun 2018;233(6):4497-4511.
149. Tabeshpour J et al. The regulatory role of curcumin on platelet functions. Journal of cellular biochemistry. Nov 2018;119(11):8713-8722.
150. Wang T et al Curcumin promotes venous thrombi resolve process in a mouse deep venous thrombosis model via regulating miR-499. Microvascular research. Jul 2021;136:104148.
151. Nemmar A et al. Protective effect of curcumin on pulmonary and cardiovascular effects induced by repeated exposure to diesel exhaust particles in mice. PLoS One. 2012;7(6):e39554.
152. Ratan ZA et al. Pharmacological potential of ginseng and its major component ginsenosides. J Ginseng Res. Mar 2021;45(2):199-210.
153. Luo BY et al. The effects of ginsenosides on platelet aggregation and vascular intima in the treatment of cardiovascular diseases: From molecular mechanisms to clinical applications. Pharmacological research. Sep 2020;159:105031.
154. Wang MM et al. Panax quinquefolium saponin combined with dual antiplatelet drugs inhibits platelet adhesion to injured HUVECs via PI3K/AKT and COX pathways. Journal of ethnopharmacology. Nov 4 2016;192:10-19.
155. Wang J et al. [Effect of Radix notoginseng saponins on platelet activating molecule expression and aggregation in patients with blood hyperviscosity syndrome]. Zhongguo Zhong xi yi jie he. Apr 2004;24(4):312-6.
156. Zuo X et al. Ginsenosides Rb2 and Rd2 isolated from Panax notoginseng flowers attenuate platelet function through P2Y(12)-mediated cAMP/PKA and PI3K/Akt/Erk1/2 signaling. Food Funct. 2021 Jul 5;12(13):5793-5805.
157. Xu ZY, Xu Y, Xie XF, et al. Anti-platelet aggregation of Panax notoginseng triol saponins by regulating GP1BA for ischemic stroke therapy. Chinese medicine. Jan 19 2021;16(1):12. doi:10.1186/s13020-021-00424-3
158. Xue Q et al. Functional roles and mechanisms of ginsenosides from Panax ginseng in atherosclerosis. J Ginseng Res. Jan 2021;45(1):22-31.
159. Yoon SJ et al. Effect of Korean Red Ginseng on metabolic syndrome. J Ginseng Res. May 2021;45(3):380-389.
160. Irfan M et al. Gintonin modulates platelet function and inhibits thrombus formation via impaired glycoprotein VI signaling. Platelets. 2019;30(5):589-598.
161. Lutomski P et al. Health properties of Yerba Mate. Ann Agric Environ Med. Jun 19 2020;27(2):310-313.
162. Yu S et al. Yerba mate (Ilex paraguariensis) improves microcirculation of volunteers with high blood viscosity: a randomized, double-blind, placebo-controlled trial. Exp Gerontol. Feb 2015;62:14-22.
163. Gebara KS, Gasparotto Junior A, Palozi RAC, et al. A Randomized Crossover Intervention Study on the Effect a Standardized Maté Extract (Ilex paraguariensis A. St.-Hil.) in Men Predisposed to Cardiovascular Risk. Nutrients. Dec 23 2020;13(1)
164. Dahmer T, Berger M, Barlette AG, et al. Antithrombotic effect of chikusetsusaponin IVa isolated from Ilex paraguariensis (Maté). Journal of medicinal food. Dec 2012;15(12):1073-80.
参考来源:
美国梅奥诊所
www.mayoclinic.org
美国血栓病学会
www.bloodclot.org
美国医疗在线网
www.webmd.com
美国卒中协会
http://www.stroke.org
加拿大心脏和卒中基金会
http://www.heartandstroke.com
免责声明和安全信息
- 本信息(包括任何附带资料)不是为了取代医生或有关合格从业人士的建议或忠告。
- 任何人如果想要对本文涉及的药物、饮食、运动或其他生活方式的使用、或改变调整,以预防或治疗某一特定健康状况或疾病,应首先咨询医生或有关合格从业人士,并获得他/她们的许可。妊娠和哺乳妇女在使用本网站任何内容前,尤其应征求医生的意见。
- 除非另有说明,本网站所述内容仅适用于成人。
- 本网站所推荐的任何产品,消费者应该以实际的产品标签内容为准,尤其应关注重要的安全信息以及产品最新信息,包括剂量、使用方法和禁忌症等。
- 由于循证医学研究、文献及有关产品处于不断的变化中,本网站工作人员将尽力更新。
- 本网站不能保证所载文章内容、综合干预方案以及相关成分或产品述及的健康益处,也不承担任何责任。

